Миотонический синдром
Содержание:
- Этиология
- Как определяется наличие дилатации
- Диагностика
- Причины, вызывающие дилатацию
- Диагностика дилатационной кардиомиопатии
- Что такое дилатационная кардиомиопатия?
- Патологическая анатомия
- Лечение
- Дилатация аорты
- Симптомы дилатации сердца
- Используемые источники
- Диагностика
- Лечение дилатационной кардиомиопатии
Этиология
Точная причина заболевания неизвестна, однако в некоторых семьях существуют несомненные доказательства его наследования. В большинстве семей, где более одного заболевшего, наиболее вероятным типом наследования является аутосомно-доминантный. Описан также по крайней мере один хорошо известный вариант аритмогенной кардиомиопатии ПЖ, который наследуется по аутосомно-рецессивному типу.
Генетическими исследованиями идентифицировано по крайне мере 7 локусов генов, ответственных за развитие заболевания. С аритмогенной кардиомиопатией ПЖ также ассоциируются мутации генов, кодирующих белки вставочных дисков (десмоплакин, плакоглобин со специфическим фенотипом, плакофилин, десмоглеин, десмоколлин). Признаки заболевания могут варьировать даже у членов одной семьи, и патология может проявиться через поколения. Считается, что занятия спортом не могут вызывать аритмогенную кардиомиопатию ПЖ, тем не менее заболевание чаще регистрируют среди спортсменов. Мутации генов рианодиновых рецепторов сердца (RyR2) ассоциируются с полиморфной желудочковой тахикардией, вызванной физическими нагрузками и ювенильной внезапной смертью.
Как определяется наличие дилатации
Незначительная дилатация – это, как правило, бессимптомная патология. Больные в таком случае не предъявляют жалоб, которые могли бы заставить подозревать наличие расширения. Но если в результате этого патологического процесса снижается насосная функция сердца, то у пациента могут проявиться признаки сердечной недостаточности: слабость, быстрая утомляемость, одышка, отеки конечностей и т. п.
Признаки дилатации можно определить по результатам ЭКГ, но выявить ее точно, только при помощи этого обследования, невозможно. Основным методом для этого служит УЗИ сердца. Оно помогает обнаружить перенесенный инфаркт или пороки сердца, а это, в свою очередь, указывает и на наличие расширения. При помощи УЗИ измеряется и диаметр желудочка (другими словами, его конечно-диастолический размер – КДР).
Правда, следует учесть, что КДР не является абсолютным показателем. При среднестатистической норме в 56 мм, он может варьироваться, в зависимости от роста, веса и физической подготовки конкретного человека. Если для двухметрового спортсмена весом более 100 кг нормой может быть и 58 мм, то для женщины, весящей 45 кг и достигающей ростом лишь 155 см, этот показатель уже признак дилатации.
Диагностика
Даже на основании физикального обследования врач может провести определенные диагностические тесты, такие как миотоническая реакция на нагрузку, воздействие холодом или другие стимуляции
Но очень важно диффенцировать эти миотонии с прогрессирующими заболеваниями, такими как миотонические дистрофии. И для дифференциального диагноза необходимы специальные методы исследования
Эти исследования включают проведение ЭМГ, который позволяет определить электрическую активность мышечных ткани; лабораторные исследования (анализы крови и анализ ДНК) биопсию мышц, которая бывает иногда необходима для окончательного диагноза мышечного заболевания.
Причины, вызывающие дилатацию
Пролапс митрального клапана
Среди причин, которые могут способствовать расширению левого предсердия, выделяют сужение или недостаточность двустворчатого клапана. Например, при пролапсе двустворчатого клапана, происходит возврат крови в предсердие при сокращении левого желудочка через неплотно прикрытое атриовентрикулярное отверстие. Таким образом, кровенаполнение предсердия в фазу его расслабления происходит не только из лёгочных вен, а еще и из левого желудочка.
Камера сердца страдает от избыточного кровенаполнения, вначале, пытаясь справиться с нагрузкой, она утолщается, а когда резервные способности истощаются — расширяется, дилатируется. При стенозе, напротив, кровь не может свободно излиться из предсердия, при его сокращении, в желудочек. Левое предсердие не опустошается полностью, остаётся полунаполненным, а в это время из лёгочных вен поступает новая порция крови — возникает перенаполнение, и как следствие расширение полости.
Стеноз митрального клапана
Помимо стеноза и недостаточности двустворчатого клапана, увеличение левого предсердия наблюдается при:
- пороках сердца,
- выраженной физической нагрузке,
- осложнениях инфекционных заболеваний (вирусных, бактериальных, грибковых),
- интоксикациях медикаментами или алкоголем, хроническом алкоголизме,
- артериальной гипертензии,
- опухолях и опухолевидных заболеваниях,
- ревматизме,
- разрыве сухожильных хорд,
- нарушениях ритма сердца,
- аутоиммунных заболеваниях,
- некоторых эндокринных нарушениях,
- дилатационной кардиомиопатии.
Диагностика дилатационной кардиомиопатии
ДКМП диагностируется как при исследовании вашей истории болезни (симптомы и семейная история), так и на основе медицинского осмотра и клинических анализов, таких, например, как анализы крови, ЭКГ, рентген грудной клетки, эхокардиография (УЗИ сердца), стресс-тест, катетеризация сердца, КТ и МРТ.
Другие анализы, чтобы выявить причину возникновения ДКМП, делают редко, т.к. при проведении биопсии миокарда, необходимо исследовать под микроскопом, образец ткани, взятый из сердца, чтобы определить причину этих симптомов.
Родственники больных дилатационной кардиомиопатией должны регулярно проходить обследование на ДКМП. Также не лишним будет генетическое тестирование, для выявления ненормальных генов.
Что такое дилатационная кардиомиопатия?
Дилатационная кардиомиопатия (ДКМП) представляет собой состояние, при котором способность сердца качать кровь снижается из-за увеличения и ослабления левого желудочка, главной насосной камеры сердца. Зачастую это не позволяет сердцу наполниться кровью, как следует. Со временем это может повлиять также на другие камеры сердца.
Симптомы дилатационной кардиомиопатии
Многие люди с ДКМП не имеют либо никаких признаков болезни, либо только незначительные симптомы, и живут абсолютно нормальной жизнью. У других же пациентов симптомы могут прогрессировать и обостряться, ухудшая тем самым работу сердца.
Симптомы дилатационной кардиомиопатии могут возникнуть в любом возрасте и включают в себя:
- симптомы сердечной недостаточности (одышка и усталость)
- отек нижних конечностей
- усталость (чувство чрезмерной усталости)
- прибавка в весе
- обморок, возникающий в связи с нерегулярными сердечными ритмами, неправильной работой кровеносных сосудов, или вовсе без какой либо причины
- учащенное сердцебиение (из-за нарушения сердечного ритма)
- головокружение — при дилатационной кардиомиопатии образуются сгустки крови из-за которых кровь течет медленнее. Если этот кровяной сгусток отрывается, он может достичь легкие (легочная эмболия), почки (почечная эмболия), головной мозг (мозговая эмболия или инсульт) или конечности (периферическая эмболия)
- боль или давление в груди(происходит обычно при физической нагрузке на организм, но также может произойти во время отдыха или после еды).
Причины дилатационной кардиомиопатии
Дилатационная кардиомиопатия может быть унаследована (семейная ДКМП), но в первую очередь эта болезнь сердца может быть вызвана рядом других факторов, в их числе:
- тяжелое заболевание коронарной артерии
- алкоголизм
- заболевания щитовидной железы
- диабет
- вирусные инфекции сердца
- аномалии клапанов сердца
- прием наркотиков
- ДКМП также может возникнуть у женщин после родов (послеродовая кардиомиопатии).
Патологическая анатомия
При морфологическом исследовании сердца вовлеченным оказывается чаще ПЖ, который имеет пятнистый вид: измененные участки могут быть окружены нормальными тканями. Вовлечение ПЖ может быть регионарным (20%) или диффузным (80%). Миокард ПЖ прогрессивно редуцируется, замещаясь жировой и фиброзной тканью, которая отличается от нефиброзной жировой инфильтрации, возникающей в ПЖ с возрастом. На ранних стадиях заболевания стенки правых отделов сердца утолщаются, но в дальнейшем из-за накопления жировой ткани и появления участков дилатации они становятся более тонкими (рис. 12.1а, б).
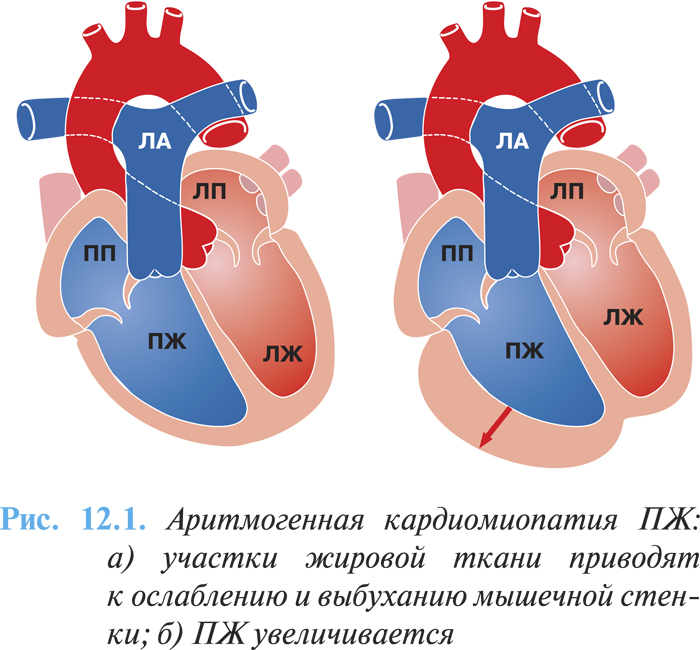
Жировое перерождение миокарда распространяется чаще от эпикардиальных слоев к эндокарду. Миокард поражается преимущественно в области выносящего тракта, верхушки и субтрикуспидальной зоны, которые рассматриваются в качестве «треугольника дисплазии».
При аритмогенной кардиомиопатии ПЖ липоматоз сопровождается преимущественно дилатацией выносящего тракта ПЖ или генерализованной дилатацией. Фибролипоматоз характеризуется наличием фокальной аневризмы ПЖ и выпячиванием в области верхушки, нижней стенки, субтрикуспидальной и инфундибулярной зоны.
По мере прогрессирования фиброзно-жировая дистрофия поражает также ЛЖ и предсердия.
Лечение
Для выбора антиаритмической терапии необходимо проведение инвазивного ЭФИ и проб с дозированной физической нагрузкой.
Среди антиаритмических препаратов эффективны амиодарон и соталол. Дигоксин применяют при тахисистолической форме фибрилляции предсердий для замедления ЧСС. Для восстановления синусового ритма проводят кардиоверсию.
Диуретики применяют при СН у больных с задержкой жидкости.
Из хирургических методов лечения применяют абляцию, если источник нарушенной электрической активности идентифицирован с помощью электрофизиологических тестов. В случаях если аритмии не контролируются с помощью лекарственных средств или абляции (обширное поражение или наличие множественных аритмогенных очагов), вшивают имплантируемый кардиовертерный дефибриллятор, в некоторых случаях требуется имплантация водителя ритма. Трансплантацию сердца применяют редко, если контроль ритма невозможен другими методами.
Дилатация аорты
Аорта – крупнейший сосуд организма, в который поступает кровь, обогащенная кислородом, из ЛЖ. Опасным состоянием является расширение (дилатация) или аневризма аорты. Обычно аорта расширяется в «слабом месте».
Одной из причин такого состояния является артериальная гипертензия. Также к патологии может привести атеросклероз и воспаление аортальной стенки.
Опасность аневризмы состоит:
- Во внезапном разрыве аорты. При этом образуется сильное внутреннее кровотечение, угрожающее жизни.
- В образовании тромбов. Это состояние также является крайне опасным для жизни.
Чаще аневризма аорты обнаруживается при обследовании случайно. Но все-таки некоторые признаки иногда присутствуют:
- Беспричинное першение в горле и кашель.
- Охриплость голоса.
- Затруднение глотания из-за сдавления пищевода.
- При разрыве аорты наблюдается сильная боль в груди, которая распространяется к шее и рукам. Прогноз в этом случае неблагоприятный – человек быстро впадает в шок из-за большой кровопотери и умирает.
Дилатация аорты не развивается моментально. Это долгий процесс, в результате которого стенка сосуда подвергается постепенному изменению. Своевременное выявление патологии может предотвратить грозные последствия заболевания.
Кроме аорты, расширению подвергаются и более мелкие сосуды. Это происходит из-за патологически увеличенного объема крови, воздействия гормонов или химических веществ. Дилатация сосудов приводит к нарушению кровообращения, что сказывается на работе всех систем организма.
Симптомы дилатации сердца
Долгое время расширение полостей сердца может не проявляться клинически за счет компенсаторной работы сердечной мышцы. По мере ослабления ее резервных возможностей возникают и прогрессируют такие признаки:
- затрудненное дыхание при физической нагрузке, в последующем – в покое;
- приступы удушья;
- кашель, мокрота с прожилками крови;
- цианоз губ, кончиков пальцев;
- отеки на ногах к вечеру;
- боль и тяжесть в правом подреберье;
- слабость, головокружение, обмороки;
- нарушение памяти;
- мерцательная аритмия, экстрасистолия, блокады проведения импульсов.
Смотрите на видео о гипертрофии левого желудочка, причинах патологии и методах лечения:
Используемые источники
- Williams B, Mancia G, Spiering W, et al. 2018 Practice Guidelines for the management of arterial hypertension of the European Society of Hypertension and the European Society of Cardiology: ESH/ESC Task Force for the Management of Arterial Hypertension. J Hypertens 2018;36(12):2284-309.
- Kawel-Boehm N, Maceira A, Valsangiacomo-Buechel ER, et al. Normal values for cardiovascular magnetic resonance in adults and children. J Cardiovasc Magn Reson 2015;17:29.
- The Task Force for the Diagnosis and Management of Hypertrophic Cardio myopathy of the European Society of Cardiology (ESC). 2014 ESC Guidelines on diagnosis and management of hypertrophic cardiomyopathy. Europ Heart J 2014;35:2733–79.
- Беленков Ю.Н., Привалова Е.В., Каплунова В.Ю. Гипертрофическая кардиопатия. М., 2011.
- Olivotto I, Girolami F, Ackerman MJ, et al. Myofilament protein gene mutation screening and outcome of patients with hypertrophic cardiomyopathy. Mayo Clin Proc 2008;83:630–8.
- Беленков Ю.Н., Привалова Е.В., Каплунова В.Ю., Фомин А.А. Гипертро фи ческая кардиомиопатия, особенности течения при длительном наблюдении. Терапевтический архив 2008;80(8):18-25. .
- Ommen SR, Maron BJ, Olivotto I, et al. Long-term effects of surgical septal myectomyon survival in patients with obstructive hypertrophic cardiomyopathy. J Am Coll Cardiol 2005;46:470–6.
- Spirito P, Pelliccia A, Proschan MA, et al. Morphology of the «athlete’s heart»assessed by echocardiography in 947 elite athletes representing 27 sports. Am J Cardiol 1994;74(8):802-6.
- Мухин Н.А., Моисеев В.С., Моисеев С.В. и др. Диагностика и лечение бо лез ни Фабри. Клин фармакол тер 2013;22(2):11-20. .
- Моисеев С.В. Поражение сердца при болезни Фабри: как заподозрить, диаг ностировать и лечить? Клин фармакол тер 2012;21(3):72-7. .
- Orteu CH, Jansen T, Lidove O, et al. Fabry disease and the skin: data from FOS, the Fabry outcome survey. Br J Dermatol 2007;157:331-7.
- Моисеев С.В., Исмаилова Д.С., Моисеев А.С. и др. Вихревидная кератопатия (cornea verticillata) при болезни Фабри. Терапевтический архив 2018;12:17-22. .
- Germain DP, Weidemann F, Abiose A, et al.; on behalf of the Fabry Registry. Analysis of left ventricular mass in untreated men and in men treated with agalsidase-beta: data from the Fabry Registry. Genet Med 2013;15(12):958-65.
- Donnelly JP, Hanna M. Cardiac amyloidosis: An update on diagnosis and treatment. Cleve Clin J Med 2017;84(12 Suppl 3):12-26.
- Patel AR, Kramer CM. Role of cardiac magnetic resonance in the diagnosis and prognosis of nonischemic cardiomyopathy. JACC Cardiovasc Imaging 2017;10(10 Pt A):1180–93.
- Wechalekar AD, Gillmore JD, Hawkins PN. Systemic amyloidosis. Lancet 2016; 387:2641-54.
- Рамеев В.В. Современные методы диагностики и лечения транстиретинового наследственного амилоидоза. Manage pain 2018;1:20-4. .
- Gillmore JD, Maurer MS, Falk RH, et al. Nonbiopsy diagnosis of cardiac transthyretin amyloidosis. Circulation 2016;133:2404–12.
Диагностика
На ЭКГ определяются:
- спонтанные желудочковые тахикардии с изменением комплекса QRS по типу блокады левой ножки пучка Гиса;
- отрицательные зубцы Т в отведениях V1–4 на фоне синусового ритма;
- уширение комплекса QRS;
- неполная блокада правой ножки пучка Гиса;
- эктопические тяжелые аритмии: желудочковая экстрасистолия, фибрилляция желудочков, предсердная тахикардия, фибрилляция предсердий.
Приблизительно у ⅓ пациентов регистрируется характерная эпсилон-волна и ППЖ.
Методом холтеровского мониторирования можно диагностировать эпизоды желудочковой тахиаритмии
Для оценки прогрессирования заболевания важно проводить регистрацию ЭКГ в динамике
При эхоКГ-исследовании выявляются:
- дилатация ПЖ и нарушение его сократимости (асинергия, диффузная гипокинезия, снижение ФВ);
- локальная аневризма ПЖ;
- повышенная трабекулярность;
- трикуспидальная регургитация;
- эмболия ЛА;
- увеличение правого предсердия;
- левые отделы сердца чаще не изменены.
С помощью допплер-эхоКГ определяется нарушение диастолической функции ПЖ и трикуспидальная регургитация. Для более точной визуализации ПЖ применяют контрастную эхоКГ миокарда.
Методом МРТ визуализируются участки замещения миокарда жировой тканью, фокальное истончение стенки и локальные аневризмы. Продемонстрирована хорошая корреляция между результатами этого метода и результатами морфологического исследования миокарда.
Для подтверждения диагноза используют рентгенконтрастную вентрикулографию, при которой выявляют дилатацию ПЖ с сегментарными нарушениями его сокращения, выпячивания контура в области дисплазии и повышение трабекулярности.
При эндомиокардиальной биопсии определяют фиброзно-жировую инфильтрацию миокарда ПЖ.
Из-за трудностей и риска проведения биопсии для подтверждения диагноза «аритмогенная кардиомиопатия ПЖ», а также неточностей в оценке структуры и функции ПЖ с помощью неинвазивных тестов Европейским кардиологическим обществом и Международным обществом и кардиологической федерацией разработаны критерии, согласно которым диагноз устанавливают при наличии 2 больших или 1 большого + 2 малых или 4 малых диагностических критериев (Corrado D. et al., 2000).
Большие диагностические критерии:
- семейный характер заболевания, подтвержденный данными аутопсии или при хирургическом вмешательстве;
- эпсилон-волна или локализованное уширение комплекса QRS (>110 мс) в правых грудных отведениях (V1–V3);
- фибролипоматозное замещение миокарда по данным эндомиокардиальной биопсии;
- значительная дилатация и снижение ФВ ПЖ при отсутствии или минимальном вовлечении ЛЖ;
- локализованная аневризма ПЖ;
- выраженная сегментарная дилатация ПЖ.
Малые диагностические критерии:
- наличие в семейном анамнезе случаев преждевременной внезапной смерти (у лиц в возрасте моложе 35 лет) вследствие предполагаемой аритмогенной кардиомиопатии ПЖ;
- ППЖ на усредненной ЭКГ;
- инвертированный зубец Т в правых грудных отведениях у лиц в возрасте старше 12 лет при отсутствии блокады правой ножки пучка Гиса;
- желудочковая тахикардия с признаками блокады левой ножки пучка Гиса, документированная по ЭКГ или результатам холтеровского мониторирования или во время нагрузочного теста;
- частые желудочковые экстрасистолы (>1000/24 ч при холтеровском мониторировании ЭКГ);
- умеренная глобальная дилатация или снижение ФВ ПЖ при неизмененном ЛЖ;
- умеренная сегментарная дилатация ПЖ;
- регионарная гипокинезия ПЖ.
Лечение дилатационной кардиомиопатии
Лечение ДКМП — это лечение хронической сердечной недостаточности (ХСН) в чистом виде, поскольку этиотропное лечение возможно лишь при известной этиологии ДКМП
Еще одной важной целью является уменьшение размеров сердца, для этого должен быть снижен уровень гормонов в крови, которые приводят к его увеличению и, в конечном счете, к ухудшению симптомов. Пациенты обычно принимают различные лекарства для лечения сердечной недостаточности. Врачи кардиологи также рекомендуют изменения в образе жизни
Какие препараты используются для лечения ДКМП?
Для улучшения работы сердца, большинство людей, принимают такие лекарства, как бета-блокаторы, ингибиторы АПФ и/или различные мочегонные средства. Если у вас аритмия, врач может дать вам лекарство для контроля сердечного ритма. Растворители крови могут быть использованы, чтобы предотвратить образование кровяных сгустков. Обсудите с вашим врачом, какое лечение вам больше подходит.
Что используют в хирургии для лечения ДКМП?
Людям с тяжелой формой дилатационной кардиомиопатии, возможно, потребуется одна из следующих операций:
- Сердечная ресинхронизирующая терапия — трёхкамерная стимуляция сердца (один электрод в правом предсердии, два — в желудочках).
- Операция окутывания сердца эластичным сетчатым каркасом — предотвращает прогрессирование ХСН, на начальных стадиях ДКМП может привести к обратному развитию заболевания.
- Механические желудочки сердца (микронасос, установленный в полости левого желудочка) — могут использоваться для временной поддержки гемодинамики, но показано, что через несколько месяцев работы аппарата улучшаются функции самого сердца.
- Трансплантация сердца — в настоящее время уже не считается средством выбора в лечении ДКМП, ввиду возможности альтернативных процедур, перечисленных выше.
Прогноз при ДКМП остается крайне серьезным — в случае идиопатической формы заболевания ежегодная летальность от 5 до 45%, для форм с известной этиологией смертность может быть меньше. Успехи в лечении привели к существенному увеличению выживаемости при этой форме кардиомиопатии.