Перинатальное поражение центральной нервной системы
Содержание:
- Также в разделе
- Профилактика
- Когда возникает гипоксически-ишемическая энцефалопатия?
- Результаты гипоксии
- Исходы и последствия ПП ЦНС
- Лечение
- Что такое перинатальная гипоксически-ишемическая энцефалопатия?
- Нейропротекторні молекули
- Каковы факторы риска и причины гипоксически-ишемической энцефалопатии?
- Лечение в клинике «Энергия здоровья»
- Лечение
- Виды поражений головного мозга
- Материалы и методы
- Как лечится гипоксически-ишемическая энцефалопатия?
- Диагностика
- Степени
- Что такое ППЦНС?
Также в разделе
| Болезнь фон Виллебранда (ангиогемофилия). Симптомы. Диагностика. Лечение. Болезнь фон Виллебранда (ангиогемофилия) — наследственное заболевание (I тип — аутосомно-доминантный тип наследования , II и III типы — аутосомно-рецессивный тип… | |
| Синдром срыгивания и рвоты. Недостаточность кардии. Кардиоспазм. Пилороспазм. Метеоризм. Острый гастрит. Вторичные (симптоматические) рвоты Синдром срыгивания и рвоты возникает у 2/3 новорождённых и может привести к аспирации и аспирационной пневмонии, асфиксии, а также дегидратации, нарушению… | |
|
Врождённые энзимопатии и экссудативная энтеропатия — целиакия, дисахаридазная недостаточность. Симптомы. Диагностика. Принципы лечения. Наиболее распространённые врождённые энзимопатии ЖКТ — целиакия и недостаточность дисахаридаз. |
|
| Круги под глазами у ребенка Круги под глазами у ребенка родители или другие родственники замечают, когда в периорбитальной зоне меняется цвет кожи, становится не таким, как обычно. Это… | |
|
Особенности выхаживания и вскармливания недоношенных детей. Отдаленные последствия недоношенности. Профилактика преждевременного рождения детей. Особенности выхаживания недоношенных Выхаживание недоношенных детей осуществляют в два этапа: в родильном доме и специализированном отделении. Затем… |
|
| Перинатальные поражения центральной нервной системы. Причины. Симптомы. Диагностика. Лечение. Профилактика. Перинатальные поражения нервной системы — группа патологических состояний, обусловленных воздействием на плод (новорождённого) неблагоприятных факторов в… | |
| Здоровый малыш — счастливая семья! Ничто так не омрачает родителей как заболевшее их чадо. А услышав диагноз «аденоидит» большинство родителей сразу же впадают в панику, начиная испробовать все… | |
| Хронический гломерулонефрит у детей. Симптомы. Диагностика. Лечение. Хронический гломерулонефрит — группа разнородных первичных гломерулопатий, характеризующихся прогрессирующими воспалительными, склеротическими и… | |
| Недоношенные дети Недоношенными считают детей, родившихся в период с 22-й по 37-ю неделю гестации с массой тела менее 2500-2700 г и длиной тела менее 45-47 см. Наиболее устойчивый показатель… | |
|
Болезнь Крона у детей. Симптомы. Диагностика. Лечение. Болезнь Крона — хроническое неспецифическое прогрессирующее трансмуральное гранулематозное воспаление ЖКТ. Чаще поражается терминальный отдел тонкой… |
Профилактика
Энцефалопатия – сложное заболевание. Не существует четкой методики, позволяющей предупредить ее появление и устранить все факторы риска. Врачи рекомендуют придерживаться следующих правил:
- обеспечить себе полноценный режим дня с чередованием труда и отдыха, полноценным ночным сном;
- минимизировать стрессы;
- правильно и сбалансировано питаться, не допускать переедания и избыточной массы тела;
- обеспечить достаточное поступление витаминов и микроэлементов;
- отказаться от курения, наркотиков, алкоголя;
- в умеренном количестве (не профессионально) заниматься спортом;
- своевременно выявлять и лечить хронические заболевания: гипертонию, сахарный диабет, атеросклероз;
- обращаться к врачу при первых признаках неблагополучия.
Когда возникает гипоксически-ишемическая энцефалопатия?
Гипоксически-ишемическоая энцефалопатия чаще развивается у доношенных новорожденных, хотя это случается также и у недоношенных детей. . Если травма происходит до 35 недели развития плода, гипоксически-ишемическая энцефалопатия, приведет к перивентрикулярной лейкомаляции (ПВЛ).
В 40 недель степень гипоксии повлияет на область поражения головного мозга; легкая гипоксия повлияет на парасагиттальной белое вещество, а тяжелая гипоксия влияет на скорлуу, таламус и парацентральное белое вещество. Область пораженного мозга будет иметь значительное влияние на симптомы, которые ребенок испытывает.
Результаты гипоксии
Нехватка кислорода для мозга может иметь такие результаты:
Тяжелая церебральная ишемия
Это состояние в четверти-половине случаев приводит к летальному исходу. Малыши не проживают и нескольких дней. Другой вариант развития событий — пневмония или другая инфекция, которая убивает ребенка чуть позже. Большинство тех, кто не умер, получают диагноз аутизма, ДЦП или слабоумия. И только у 10% выживших не отмечается последствий.
Средняя ишемия
Тяжелые отдаленные последствия, согласно статистике, имеют от 30 до 50% малышей.
Ишемия легкой степени
Исход в большинстве случаев благополучный, инвалидизации не отмечается.
Исходы и последствия ПП ЦНС
Последствия ПП ЦНС можно определить к 1 году жизни. Ниже представлены основные их проявления:
- Нарушение моторного развития: задержка приобретения навыков удерживания головы, переворотов, сидения, ползания, вставания, самостоятельной ходьбы относительно физического возраста ребенка.
- Формирование парезов и параличей как одной, так и нескольких конечностей (моноплегия, диплегия, гемипарез, тетрапарез), которые относятся к различным формам детского церебрального паралича.
- Нарушение психо-речевого развития: задержка приобретения навыка гуления, лепета, первых слов и фраз, качество произносимых звуков, сроки формирования пинцетного захвата и указательного жеста, понимание обращенной речи, интерес к окружающим предметам и использование их по назначению, характер игры, запоминание новой информации, концентрация внимания с формированием синдрома дефицита внимания с гиперактивностью.
- Нарушение поведения и эмоций: сроки формирования комплекса оживления, дифференцировка родных и чужих, эмоциональный резонанс, степень выраженности эмоций, общение со сверстниками и взрослыми, возможность совместной игры, формирование навыков опрятности, возможно приводящие к расстройствам аутистического спектра.
- Гидроцефалия: избыточный прирост окружности головы, деформация головы, выраженность подкожных вен в височных областях, признаки гипертензионного и гидроцефального синдромов.
- Пароксизмальные состояния не эпилептического генеза: аффективно-респираторные приступы, доброкачественный миоклонус младенчества ( синдром Фиджермана), доброкачественные неонатальный миоклонус сна, синдром Сандиффера, младенческий тортиколис, беспокойный сон, ночные страхи, ритмичные движения во сне (раскачивания, мотание головой, сосание пальца, скрежет зубов).
- Возрастзависимые эпилептические синдромы: ранняя инфантильная эпилептическая энцефалопатия ( синдром Отахара), ранняя миоклоническая энцефалопатия, синдром Драве, синдром Веста, доброкачественные неонатальные эпилептические синдромы, доброкачественная миоклоническая эпилепсия младенчества, доброкачественная парциальная эпилепсия младенчества.
Лечение
Чем раньше будет начато лечение энцефалопатии, тем больше шансов остановить прогрессирование патологии и восстановить полноценную работу головного мозга.
В первую очередь, необходимо устранить причину поражения нейронов:
- скорректировать уровень сахара в крови;
- стабилизировать артериальное давление;
- восстановить работу печени, почек, поджелудочной железы;
- снизить уровень холестерина в крови;
- вывести токсины;
- нормализовать уровень гормонов и т.п.
Лечение непосредственно энцефалопатии требует назначения препаратов, улучшающих кровоток в сосудах головного мозга и обмен веществ внутри клетки. В зависимости от причины и степени поражения, врачи могут назначить:
- ноотропы (церебролизин, пирацетам): направлены на усиление метаболизма;
- кроворазжижающие средства (аспирин, пентоксифиллин и т.п.): способствуют ускорению кровотока, препятствуют образованию тромбов;
- антиоксиданты: нейтрализуют токсины;
- ангиопротекторы (кавинтон, никотиновая кислота и другие): необходимы для ускорения кровообращения и обмена веществ;
- витаминно-минеральные комплексы, аминокислоты;
- симптоматические средства: успокоительные, противосудорожные препараты и т.п.
При энцефалопатии курсы лечения проводятся регулярно, минимум 2 раза в год. Это позволяет держать заболевание под контролем. Подбор конкретных препаратов и определение дозировки осуществляется только врачом. Единой схемы лечения для всех больных не существует.
Для усиления действия лекарственных препаратов используются немедикаментозные методы лечения:
- физиотерапия (рефлексотерапия, электрофорез, магнитотерапия, лазерная терапия);
- лечебная физкультура для улучшения состояния мышц, облегчения контроля за ними;
- массаж для расслабления и улучшения кровообращения;
- иглоукалывание.
В отдельных случаях (при сосудистой природе энцефалопатии) приходится прибегать к хирургическому лечению:
- устранение тромба из просвета сосудов;
- расширение суженных участков артерии с установкой стента, поддерживающего стенки в правильном положении;
- шунтирование: восстановление кровотока за счет создания альтернативного пути, обходящего пораженный участок.
Что такое перинатальная гипоксически-ишемическая энцефалопатия?
Перинатальная гипоксически-ишемическая энцефалопатия (ГИЭ) – это следствие недостаточного кровоснабжения головного мозга ребенка во время беременности матери, родов или в течение первого месяца его жизни. Гипоксия-ишемия головного мозга является основной причиной неврологических повреждений у новорожденных. Одними из основных параметров, характеризующих тяжесть гипоксически-ишемического поражения головного мозга в родах и во время беременности, являются оценка по шкале Апгар и наличие мекония в околоплодных водах.
Последствия ГИЭ могут быть различными: от незначительного снижения внимания и неусидчивости ребенка до тяжелых форм детского церебрального паралича.
Дети с умеренной степенью поражения мозга могут выглядеть здоровыми в течение первых дней и даже месяцев жизни. Патология у них выявляется при проведении УЗИ головного мозга на первом месяце жизни, при осмотре неврологом и другими специалистами.
Детям с тяжелой формой ГИЭ и асфиксией в родах, как правило, требуется интенсивная терапия, и они проходят поэтапное лечение в родильном доме и отделении патологии новорожденных.
Перинатальная гипоксически-ишемическая энцефалопатия умеренной и тяжелой степени является одним из основных факторов риска развития ДЦП.
Течение ГИЭ очень индивидуально, но, как правило, оно сопровождается гибелью части клеток головного мозга и требует своевременного и правильного лечения. Соблюдение этого принципа позволяет добиться существенного улучшения даже при тяжелом поражении головного мозга.
Нейропротекторні молекули
В експериментальних дослідженнях проаналізовано різні нейропротекторні молекули, які мають терапевтичний потенціал при ГІЕ: мелатонін, остеопонтин, інтерферон-, едаравон тощо .
Показано, що мелатонін (N-ацетил-5-метокситриптамін), ендогенний індоламін, має антиоксидантні, протизапальні та антиапоптотичні властивості . Мелатонін вільно проникає крізь плаценту і гематоенцефалічний бар’єр, що робить його привабливим для нейропротекції при ГІЕ. Ефективним та доцільним виявилося внутрішньовенне введення мелатоніну і терапевтична гіпотермія всього тіла новонародженого з ГІЕ . Як свідчать результати багатьох досліджень, комбінована терапія має більший ефект, тому перспективним є використання мелатоніну як додаткового агента при лікуванні ГІЕ як у доношених, так і у недоношених новонароджених . Однак до впровадження у клінічну практику необхідно дослідити оптимальні дози і тривалість прийому мелатоніну.
Остеопонтин — багатофункціональний глікопротеїн, який має як про-, так і протизапальні властивості . Показано, що максимальна ендогенна експресія остеопонтину в мозку новонароджених спостерігається у першу добу і поступово зменшується до 21-ї доби постнатального періоду. При ГІЕ ендогенна експресія остеопонтину збільшується і досягає максимуму через 48 год. Введення екзогенного остеопонтину зменшує зону інфаркту та поліпшує неврологічні показники через 7 тиж після ГІЕ . Остеопонтин відновлює структуру головного мозку після гіпоксично-ішемічного ушкодження новонароджених шляхом регулювання проліферації клітин мозку, виживання клітин та диференціювання олігодендроцитів .
Інтерферон-β. Запалення відіграє важливу роль у патології ГІЕ, тому заходи, спрямовані на зменшення запалення, можуть бути корисними при лікуванні цієї патології. На моделі оклюзії середньої мозкової артерії показано, що інтрастріатальні ін’єкції інтерферону-β зменшують розмір зони ішемії і блокують проникнення клітин, які сприичняють запалення . Інші дані отримано на моделі фокальної ішемії . Внутрішньовенне введення у хвостову вену інтерферону-β не мало позитивного ефекту, що може свідчити про його неспроможність проникати крізь гематоенцефалічний бар’єр. Цей факт слід ураховувати при використанні інтерферону-β для лікування ГІЕ .
Едаравон — акцептор вільних радикалів, який взаємодіє з перекисними і гідроксильними радикалами, формуючи стабільні продукти окиснення . Продемонстровано ефективне застосування едаравону як потужного антиоксиданта при ГІЕ . Показано, що системне введення едаравону через 30 хв після реанімаційних заходів при ГІЕ може врятувати нейрони смугастого тіла на моделі ГІЕ новонароджених . Установлено, що внутрішньочеревне введення едаравону в гострій фазі ГІЕ поліпшувало пам’ять і здатність до навчання протягом декількох днів після ГІЕ .
Каковы факторы риска и причины гипоксически-ишемической энцефалопатии?
Асфиксия является наиболее значимым фактором риска для ГИЭ. От степени и продолжительности кислородного голодания зависит, разовьется гипоксически-ишемическая энцефалопатия или нет, и насколько серьезными будут последствия. Факторы, могут привести к асфиксии:
- Острая гипотония матери
- Кровь, содержащая меньше кислорода из-за плохо функционирующих легких
- Осложнения со стороны сердца
- Травмы от клинически узкого таза
- Травмы от осложнений со стороны пуповины
- Нарушение кровоснабжения мозга во время родов
- Остановка дыхания или гипоксия
- Кровотечение в родах
- Медицинская халатность
- Выпадение пуповины
- Отслойка плаценты
- Давление на череп с изменение его формы, в результате чего развивается кровотечение или ишемия
- Низкое предлежание плаценты
- Стресс во время родов
- Травма
- Разрыв матки
Инсульт плода также увеличивает вероятность развития гипоксии-ишемической энцефалопатии. Факторы, которые могут привести к инсульта плода включают в себя:
- Нарушения свертывания крови
- Нарушение кровотока в плаценте
- Аномальные кровеносные сосуды, которые могут привести к разрыву
- Высокое или низкое давление у матери
- Инфекции у матери, особенно воспаление тазовых органов
Лечение в клинике «Энергия здоровья»
Врачи клиники «Энергия здоровья» всегда готовы принять пациента любого возраста. Мы проведем тщательное обследование, выявим возможные причины энцефалопатии и примем все меры по ее устранению:
- назначим наиболее подходящую терапию, распишем курс лечения и частоту его повторения;
- проведем все необходимые манипуляции (постановка капельницы, внутривенные и внутримышечные инъекции) в комфортабельных условиях дневного стационара и манипуляционного кабинета;
- дополним терапию современными физиотерапевтическими процедурами;
- проведем курс массажа и назначим ЛФК для максимальной эффективности.
Наши неврологи будут контролировать состояние пациента и корректировать лечение при необходимости. Лечение энцефалопатии – это длительный и сложный процесс, но мы готовы за него взяться.
Лечение
На сегодня специфическая терапия, «оживляющая» умершие клетки головного мозга, не разработана. Существуют медицинские методы, которые останавливают процесс гипоксии и отмирания, чтобы ребенок не умер.
Лечение острого ишемического периода
Как уже было отмечено, церебральная ишемия тяжелая и средняя дают о себе знать сразу, симптомы специфичны. При отсутствии самостоятельного дыхания в первые 2 минуты жизни (а также при отсутствии дыхания с кислородной маской) нужно проводить реанимацию. делают интубацию и ИВЛ. Если повреждены небольшие участки мозга, то через 2-3 минуты после начала реанимации малыш уже дышит сам. Тогда ребенка дают маме. Такого маленького пациента наблюдают.
Если же реанимация занимает больше времени, то малыша относят в отделение интенсивной терапии. Там нужно постоянно следить за показаниями состояния организма, в том числе, за количеством глюкозы и гемоглобина в крови, за уровнем газов, за процессами кровообращения и биения сердца новорожденного. Для этого существует специальная аппаратура.
Противосудорожная терапия заключается в назначении специальных препаратов, например, фенитоина. Доза подбирается врачом индивидуально. Это помогает остановить судороги, и мозг не повреждается в дальнейшем. Поскольку ишемия оказывает негативное влияние не только на мозг, а страдает и сердце, то нужна специальная терапия и для этого органа. Чтобы сердечко маленького пациента не остановилось, ему вводятся добутамин и допамин.
На сегодня актуальны данные исследований о том, что температура, которая на 3-4 градуса меньше нормальной, может спасти участки мозга от отмирания, что предупреждает инвалидизацию и летальный исход. Этот метод получил название гипотермической терапии. Она практикуется не так давно, всего лишь с 2010-го года. Нужно, чтобы процесс контролировали опытные врачи. Пациента согревают постепенно.
Лечение последствий
Как уже было сказано выше, для ребенка всегда есть последствия при церебральной ишемии тяжелой и даже средней степени. Это может быть только синдром дефицита внимания. Но в других случая отмечают умственную отсталость и ДЦП. Если есть судороги, применяются специальные препараты, купирующие их. Назначаются врачом в индивидуальной дозировке, самолечение категорически запрещено.
Если у малыша появился тяжелый церебральный паралич со спастичностью конечностей, то для облегчения ситуации принимают миорелаксанты. Какие бы последствия ни были, лекарствами лечение не ограничится. Важна ежедневная реабилитация. Детям с ДЦП проводят специальные курсы массажа. Это должен делать специалист. В домашних условиях можно делать лишь часть упражнений, которые покажут родителям специалисты. Детям более старшего возраста, которые имеют диагноз ДЦП вследствие церебральной ишемии, нужна ЛФК.
Коррекция неправильные поз проводится с помощью специальных приспособлений: колясок, валиков, лонгет, специальных стульев. Если есть спастичность, ручки и ножки больного малыша могут стать не физиологично. Этого лучше избежать.
В нашей стране мало специалистов, которые могут адекватно вылечить последствия церебральной ишемии у новорожденных. Имеет место гипердиагностика. У детей в возрасте до 6 мес могут быть симптом Грефе, повышение тонуса мышц и вздрагивания. И доктора могут подумать, что это проявления энцефалопатии. Соответственно, назначат ненужное на самом деле лечение.
Новорожденных нельзя осматривать, когда они находятся в сонном состоянии или чем-то испуганы. Тогда также можно диагностировать неврологические патологии, которых нет. К ненужным препаратам, которые могут назначаться по ошибке, относятся:
- сосудистые
- ноотропы
- гомеопатия
Виды поражений головного мозга
Поражение головного мозга может быть как очаговым, так и диссеминированным. Давайте разберёмся, что такое очаговое поражение головного мозга. Это состояние, при котором имеется чётко отграниченный единичный очаг с некротизированными тканями, т.е. это локальное поражение мозга. Такой вид повреждения часто формируется при остром нарушении мозгового кровообращения.
Диссеминированное или мультифокальное поражение головного мозга – вид повреждения, при котором обнаруживаются множественные разрозненные очаги повреждения тканей головного мозга. Мультифокальная форма встречается при инфекционных заболеваниях головного мозга, например при занесении инфекционного агента гематогенным путём в мозговое вещество или при онкологическом поражении.
Материалы и методы
В отделении детей младшего возраста НИИАП ФГБОУ ВО РостГМУ МЗ РФ были обследованы 120 детей в возрасте от 6 до 8 лет с последствиями перинатальной патологии ЦНС гипоксически-ишемического генеза, в основном, дети дошкольного возраста (61,7 %). Количество мальчиков преобладало над количеством девочек в обеих возрастных группах (78,0 %).
В числе обследованных выделены три группы. В первую группу вошли дети с церебрастеничежим синдромом — 30 детей (25 %); вторую группу составили пациенты с синдром гиперактивности и дефицита внимания (СДВГ) — 58 детей (48,3 %); третью группу — дети с детским церебральным параличом (ДЦП), спастической ди- плегией — 32 ребенка (26,7 %).
Критериями отбора во все группы были данные анамнеза о неблагоприятном течении беременности и родов, оценка по шкале Апгар при рождении (не более 5 — 7 баллов), неврологическая симптоматика в раннем неонатальном периоде и на первом году жизни, интеллектуальная сохранность детей, наличие мотивации к занятиям ЭЭГ-БОС-тренингом, отсутствие на предварительном диагностическом ЭЭГ-исследовании грубых очаговых нарушений, генерализованных разрядов, пик-медленных волн. из числа обследованных детей исключены пациенты с пороками и аномалиями развития ЦНС, хромосомной и моногенной патологией, эпилепсией, а также пациенты, имеющие членов семьи с клиническими проявлениями СДВГ. Все пациенты регулярно наблюдались неврологом 1 раз в 3 — 6 месяцев и 2 раза в год получали нейропротективные, вазоактивные и метаболические средства в сочетании с физиотерапией, лФК и лечебным массажем, психо-логопедической коррекцией.
Обязательным исследованием перед началом БОС- терапии и после его проведения была психодиагностическая оценка функций произвольного внимания по шкале Тулуз-Пьерона (в адаптации л.А. ясюковой) , которая относится к корректурным пробам и позволяет измерить показатели объема, концентрации и устойчивости внимания, а также сопоставлять изменения показателей внимания в динамике.
Запись ЭЭГ осуществлялась на электроэнцефалографе — анализаторе ЭЭГА 21/26 «Энцефалан-131-03», модификация 10 (Производитель: ООО НПКФ «Медиком МТД», Россия). ЭЭГ регистрировалось перед началом лечения по схеме «10 — 20» в лобных, височных, центральных отведениях в течение 30 мин. с проведением сравнительной характеристики выявленных нарушений ЭЭГ (классификация людерса) между группами .
ЭЭГ-БОС-тренинг по коррекции β-ритма проводился количеством 15 сеансов длительностью 20 — 30 минут ежедневно на аппарате «Кинезис» («Нейротех», Россия). Данная методика предполагает индивидуализированный подход и возможность изменения протокола при повышенной утомляемости ребенка во время сеанса, что связано с нагрузкой при выполнении заданий программы.
От официальных представителей пациентов получено письменное добровольное информированное согласие на участие в исследовании. Проведение исследования одобрено этическим комитетом ФГБУ НИИАП, протокол №10 от 21.03.2017.
Для проведения статистического анализа полученных показателей до и после лечения использовался критерий значимости для сравнения двух пропорций (долей) в предположении, что переменные распределены по нормальному закону (пакет СТАТИСТИКА 6.0).
Как лечится гипоксически-ишемическая энцефалопатия?
Лечение гипоксически-ишемической энцефалопатии сосредоточено на оказании помощи ребенку адаптироваться к нарушениям, которые возникают в результате травмы головного мозга. Методы реабилитации обычно используются для лечения церебрального паралича, вызванного гипоксической-ишемической энцефалопатией.
Асфиксия обычно вызывает стойкое повреждение, которое иногда продолжает прогрессировать даже после выхода из асфиксии. Чтобы предотвратить дальнейшее повреждение ребенка может быть медицинской контролировать, чтобы:
- Поддержание нормального уровня глюкозы в крови
- Поддержание нормального артериального давления
- Предотвращение или контроль за судорогами
- Предотвратщение или минимизация отека мозга
Диагностика
В основном врачи находят ишемию у младенца в первые несколько дней после родов. Если степень кислородного голодания тяжелая, то у ребенка может быть нормальное состояние 3-4 часа или даже несколько суток, а потом резко наступает очень плохое состояние
Потому важно полностью обследовать малыша
Осмотр малыша. Врачи дают оценку ситуации пациента по шкале Апгар, о которой говорилось выше. Для этого проверяют рефлексы, меряют вес тела и рост.
Анализы:
- общий анализ крови
- электролиты
- свертываемость
- газы
Проводится магнитно-резонансная томография, если ишемия мозга тяжелая или умеренной степени. МРТ почти не применяется при легкой степени церебральной ишемии у новорожденного. С помощью ультразвука нельзя точно определить энцефалопатические процессы, и стоит учитывать, что результат может быть ложноположительным. УЗИ может применяться для постановки первичного диагноза, но обязательно проводятся другие исследования.
Актуален метод электроэнцефалографии, сокращенно — ЭЭГ. Обязательно для детей с тяжелой степенью рассматриваемой патологии. ЭЭГ дает возможность обнаружить скрытые судороги. Также метод показывает, насколько мозг поврежден, насколько он может быть активен. Также ЭЭГ делают, чтобы выбрать адекватное лечение.
Степени
При легкой степени ишемии повышается мышечный тонус, но не слишком сильно. Сухожильные глубокие рефлексы у таких детей усиливаются. Они плохо сосут грудь, постоянно плачут или, наоборот, спят постоянно. На протяжении первых 3 суток жизни проявления патологии ликвидируются. У детей, которые не пробыли 9 месяцев в животе матери, могут быть не повышенные, а сниженные рефлексы и тонус мышц.
средняя
— частые апноэ
— сниженный хватательный и сосательный рефлекс
— вялый рефлекс Моро
— сниженные сухожильные рефлексы
— слабый тонус мышц
Симптоматика при средней степени ишемии у новорожденных появляются в первые 24 часа после родов. Врачи говорят о благоприятном прогнозе, если на протяжении 14 дней симптоматика ишемии исчезла.
тяжелая
— несогласованные движения глаз
— косоглазие, нистагм
— отсутствие рефлексов, которые в норме должны быть у новорожденного
— нерегулярное дыхание, таких детей приходится подключать к аппарату искусственной вентиляции легких
— ступор или кома
— судороги
— скачки артериального давления (АД)
— нарушения сердечного ритма
Что такое ППЦНС?
Само словосочетание перинатальный период говорит о том, что перинатальное поражение ЦНС развивается у еще не родившегося или только появившегося на свет ребенка.Перинатальное поражение центральной нервной системы (ППЦНС) — это не один, а несколько диагнозов, которые подразумевают нарушение функций работы в головном мозге новорожденного ребенка и могут привести к стойким неврологическим последствиям в более старшем возрасте (например, ДЦП, ЗПРР).
Весь перинатальный период условно делится на три этапа:
– с 28 недели и до момента родов длится антенательный период;
– сам процесс родов называется интранатальным периодом;
– неонатальный период это промежуток времени с момента рождения до 7 дня жизни включительно.
В современной медицине нет точного названия заболевания при поражении ЦНС плода, есть только сборное, его называют ППЦНС или же перинатальная энцефалопатия. Перинатальное поражение ЦНС у новорожденных, проявляется нарушениями в работе двигательного аппарата, нарушением речи и психики.
С развитием медицины, перестали данный диагноз употреблять для детей старше одного месяца. По истечении месяца врач должен поставить точный диагноз ребенку. Именно в этот период невролог с точностью определяет, насколько сильно повреждена нервная система. Назначает лечение и следит за тем, чтобы оно было подобрано правильно.
Каковы причины и факторы риска ППЦНС?
Причины, по которым может развиться перинатальное поражение центральной нервной системы достаточно разнообразны, среди самых популярных:
– соматическое заболевание матери, которое сопровождается хронической интоксикацией;
– наличие острых инфекционных заболеваний или хронических очагов инфекции, в то время когда будущая мать вынашивала ребенка;
– в случае, если у женщины нарушен процесс питания, или же она не созрела для беременности и родов;
– нарушение маточно-плачцентарного кровотока во время беременности;
– изменения в обмене веществ также влечет за собой расстройство нервной системы у будущего ребенка (повышение уровня биллирубина, неонатальная желтуха);
– в случае сильного токсикоза, как на ранней стадии, так и на поздней, или появление иных проблем с вынашиванием ребенка;
– окружающая среда выступает немаловажным фактором в развитии заболевания;
– появление патологии во время родов — это может быть слабая родовая деятельность, ускоренные роды;
– если ребенок рождается недоношенным, то и его организм не развит полностью, поэтому на данном фоне может появиться нарушение в работе ЦНС;
– наибольшему риску развития поражений ЦНС подвержены малыши, у которых присутствует наследственный фактор.
Все остальные причины возникновения ППЦНС ситуативные и в большей степени предугадать их появление просто нельзя.
Выделяют несколько путей развития перинатального поражения ЦНС у новорожденных детей в зависимости от причины и последующей симптоматики, анализ которых позволяет поставить первоначальный диагноз: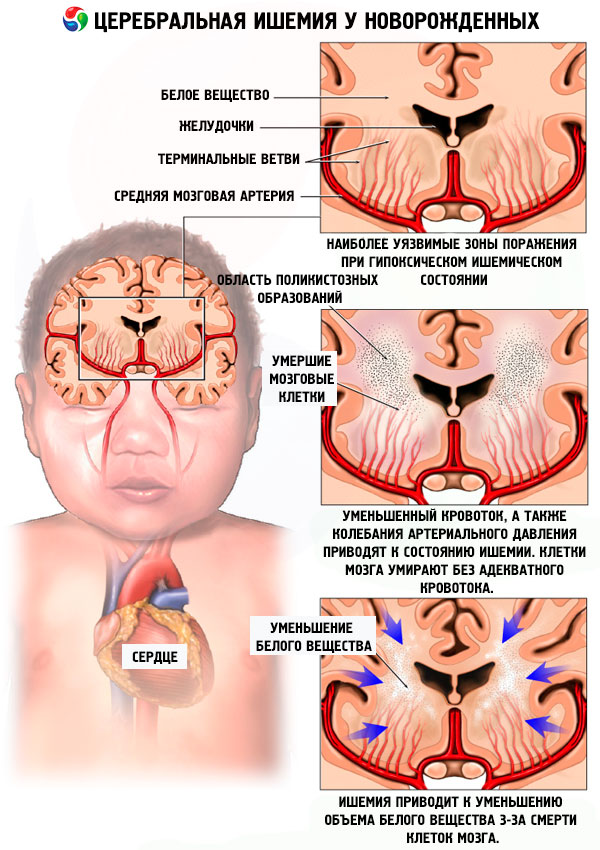
– Если четко зафиксирован недостаток кислорода, во время нахождения малыша внутри организма матери (гипоксия), то диагностируют гипоксическое поражение ЦНС.
– Во время родов у младенца может быть повреждена тканевая структура (это может быть как головной мозг, так и спинной). В этом случае, уже идет речь о травматическом поражении ЦНС, в результате чего появляются изменения в работе головного мозга.
– В случае нарушения обмена веществ могут появиться метаболические и токсико-метаболические поражения. Это может быть связано с употреблением во время беременности алкоголя, лекарственных препаратов, никотина.
– Изменения в ЦНС при наличии инфекционных заболеваний перинатального периода.