Автореферат и диссертация по медицине (14.00.28) на тему:артериовенозные мальформации вены галена (клиника, диагностика, тактика хирургического лечения)
Содержание:
- КЛИНИЧЕСКАЯ ДИАГНОСТИКА ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ
- Лучевое лечение АВМ головного мозга
- Общие сведения о болезни
- Метод лечения артериовенозной мальформации головного мозга
- Нюансы диагностики венозных мальформаций
- Нюансы диагностики венозных мальформаций
- Диагностика ангиодисплазии конечности
- Проявления аномалий венозных сосудов
- Клиническая картина и симптоматика артериовенозных мальформаций сосудов головного мозга (АВМ)
- Принципы микрохирургического удаления АВМ
- Уход
- Диагностика
- Дуплексная допплеровская ультрасонография
- Виды церебральных мальформаций венозно-артериального русла
- Заключение
КЛИНИЧЕСКАЯ ДИАГНОСТИКА ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ
При физикальном обследовании легко заметить асцит, желтуху, паукообразные ангиомы на коже, эритему ладоней, атрофию яичек, гинекомастию, контрактуры Дюпюитрена и атрофию мышц. Могут также наблюдаться признаки портосистемной энцефалопатии — в тяжелых случаях астериксис (хлопающий или “порхающий” тремор кистей) и летаргия, в легких — раздражительность, нарушения сна. У большинства больных с ПГ имеется также спленомегалия, хотя размер селезенки слабо взаимосвязан с портальным венозным давлением и ее увеличение может быть вызвано другими заболеваниями. На гипердинамическое состояние могут указывать высокий (скачущий) пульс, теплые конечности (хорошее кровоснабжение) в сочетании с артериальной гипотензией.
О наличии портосистемных коллатералей свидетельствуют дилатированные вены живота (умбиликально-эпигастральные шунты) и “голова медузы”, представляющая собой извилистые коллатеральные вены вокруг пупка. Внутренние геморроидальные узлы не являются специфической находкой, но также могут быть признаком коллатерализации. При этом видимые коллатеральные сосуды на спине указывают не на портальную гипертензию как таковую, а на обструкцию на уровне нижней полой вены. Ее редкой причиной может быть компрессия нижней полой вены узлами регенерации при циррозе печени.
Асцит легко выявить при большом количестве жидкости — в таких случаях живот плотный, имеется симптом баллотирования. Однако при незначительном объеме жидкости наличие асцита подтверждается инструментально, например, с помощью ультрасонографии. Парацентез помогает установить причины асцита: о его портальной (неперитонеальной) этиологии свидетельствует сывороточно-асцитический градиент альбумина (SAAG) свыше 1,1 г/дл (11 г/л). Однако данный метод не позволяет различить печеночную и надпеченочную ПГ, например, при застойной сердечной недостаточности. Последние исследования свидетельствуют о снижении SAAG после установки трансюгулярных портосистемных шунтов (TIPS).
Результаты лабораторных проб при ПГ, в целом, не специфичны. Отмечается удлинение протромбинового времени и тромбоцитопения. У больных циррозом печени данные показатели считаются предикторами наличия пищеводных варикозно расширенных вен (см. ниже). Гипоальбуминемия указывает на тяжесть поражения печени и непрямо — на ПГ. Аналогично гипонатриемия и низкая концентрация натрия в моче могут быть следствием задержки воды и натрия в организме при синдроме портальной гипертензии.
Лучевое лечение АВМ головного мозга
|
Leksell Gamma Knife |
Лучевая терапия (гамма-нож, облучение протонным пучком) наиболее эффективна при маленьких компактных мальформациях диаметром не более 3 см. Так, при мальформациях менее 1 см в диаметре полной облитерации можно достичь почти в 90 % случаев, а при мальформациях диаметром более 3 см лишь — до 30%. Отрицательной стороной лучевой терапии АВМ является то, что облитерация сосудов АВМ наступает спустя 1–3 года после лечения. Как показали недавние исследования, предварительная эмболизация АВМ снижает эффективность радиохирургии. По данным НИИ нейрохирургии после стереотаксического облучения полной облитерации удается достичь в более чем 70% случаев. У 10% больных наблюдается уменьшение размеров АВМ и редукция кровотока.
Общие сведения о болезни
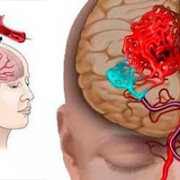
Аневризма вены Галена – это патология крупной вены, проходящей рядом со зрительными буграми через пространство, внутри которого находится спинномозговая жидкость
Аневризма вены Галена – это патология крупной вены, проходящей рядом со зрительными буграми через пространство, внутри которого находится спинномозговая жидкость. Это пространство располагается среди оболочек мозга спины и головы и называется цистерной Галена. Эта патология представляет собой разнообразные аномалии кровеносной системы мозга, которые связаны с нарушением формирования большого сосуда мозга в эмбриональном состоянии. Они выражаются в появлении разнообразных сосудистых мальформаций, начиная от переплетения патологических артерий, образовавших клубочки и заканчивая выпучиванием стенок вены Галена.
У аномальных сосудов очень тонкие стенки, имеющие собственное строение, не похожее на состав вены или артерии. Слои стенок аномальных сосудов имеют в своем составе гиалиновые и коллагеновые волокна. Сосудистые мальформации – это врожденные заболевания головного мозга, которые появляются в эмбриональном периоде. Сосудистые мальформации, то есть клубки различных форм и размеров, образовавшиеся в результате переплетения аномальных сосудов, не имеют капилляры, из-за чего кровоток движется из артерий прямиком в вены. В результате данного патологического процесса нарушается кровоснабжение тканей. И вследствие недостаточного притока крови к головному мозгу, происходит деформация обменных тканевых процессов и развитие патологии вены Галена.
Одной из самых опасных аномалий в данном случае является аневризма вены Галена, которая приводит к изменению тканевой структуры сосуда, из-за чего тот теряет привычную эластичность. И в итоге может произойти разрыв вены, что приведет к кровоизлиянию в мозг и смерти. Также при аневризме возникает деформация сосудов, которая также представляет серьезную опасность, так как кровь проникает в новообразования, провоцируя изменение их размеров. И появившиеся выпячивания оказывают давление на мозг. Аневризма вены Галена – это редкое заболевание, встречающееся только у 1% населения планеты, в основном у мальчиков.
Несмотря на редкие случаи диагностирования болезни, данная проблема является довольно актуальной и изучаемой по причине большого количества летальных исходов, практически в 90% случаев. И хоть сосудистая нейрохирургия активно развивается, уровень смертности при аневризме вены Галена снизился незначительно. Такой высокий уровень смертности в данном случае можно объяснить неготовностью многих врачей столкнуться с данной проблемой ввиду ее редкой встречаемости.
Метод лечения артериовенозной мальформации головного мозга
Для выбора наиболее адекватного метода лечения артериовенозной мальформации, Мартин и Шпецлер изобрели шкалу бальной оценки АВМ, в которой учитываются следующие признаки:
- Размер АВМ: до 3 см — 1 балл, 3-6 см — 2 балла, более 6 см — 3 балла;
- Локализация в функционально значимой зоне: Да — 1 балл, нет — 0 баллов;
- Дренирование в крупные венозные коллекторы — в вену Галена, ВСС, поперечный синус. Да — 1 балл, нет — 0 баллов.
Таким образом пациенты с количеством баллов 1-2 могут подвергнуться только операции, 3-4 подлежат эндоваскулярному вмешательству с последующей открытой хирургической операцией, 5 — только эндоваскулярному лечению или наблюдению.
Кроме того АВМ до 3-4 см в диаметре могут быть подвергнуты радиохирургии, в результате которой происходит выключение АВМ из кровотока в течение 2 лет за счет развития воспаления и пролиферации эндотелия с последующей облитерацией сосудистого русла.
Нюансы диагностики венозных мальформаций
Диагностика патологии внутричерепных вен осуществляется посредством:
- Рентгеноконтрастной ангиографии — после рождения малыша это основной метод исследования, играющий решающее значение в определении хирургической тактики;
- Ультразвукового анализа с допплерометрией — до родов в третьем триместре и после рождения малыша (нейросонография) это самый безопасный и наиболее доступный способ диагностики;
- КТ, МРТ — в раннем неонатальном периоде.
Если женщина не обследовалась до родов, то заподозрить патологию крайне сложно и по причине редкой встречаемости, и вследствие отсутствия в части случаев клинических признаков в момент рождения ребенка. Педиатры ставят диагноз методом исключения иных причин водянки мозга и недостаточности сердца.
Помимо ультразвуковой диагностики, применяются компьютерная и МР-томография, которые показывают клубки аномально развитых внутричерепных сосудов. Уточнить характер ветвления эмбриональных сосудов, их взаимоотношения с нормальными, наличие или отсутствие тромбозов дает возможность рентгеноконтрастная ангиография, по итогам которой также разрабатывается план оперативного лечения.
Нюансы диагностики венозных мальформаций
Диагностика патологии внутричерепных вен осуществляется посредством:
- Рентгеноконтрастной ангиографии — после рождения малыша это основной метод исследования, играющий решающее значение в определении хирургической тактики;
- Ультразвукового анализа с допплерометрией — до родов в третьем триместре и после рождения малыша (нейросонография) это самый безопасный и наиболее доступный способ диагностики;
- КТ, МРТ — в раннем неонатальном периоде.
Если женщина не обследовалась до родов, то заподозрить патологию крайне сложно и по причине редкой встречаемости, и вследствие отсутствия в части случаев клинических признаков в момент рождения ребенка. Педиатры ставят диагноз методом исключения иных причин водянки мозга и недостаточности сердца.
Помимо ультразвуковой диагностики, применяются компьютерная и МР-томография, которые показывают клубки аномально развитых внутричерепных сосудов. Уточнить характер ветвления эмбриональных сосудов, их взаимоотношения с нормальными, наличие или отсутствие тромбозов дает возможность рентгеноконтрастная ангиография, по итогам которой также разрабатывается план оперативного лечения.
Диагностика ангиодисплазии конечности
Врачи Сосудистого центра имени Н.И. Пирогова проводят тщательное обследование сосудов вен нижних конечностей, чтобы точно определить степень поражения заболеванием. Применяется поэтапное комплексное обследование:
- Визуальное – врач осматривает конечность и оценивает характер патологии.
- Ангиография – в поражённый сосуд вводят реагент и проводится рентгенологическое обследование.
- Томографическая ангиография – предоставляет объёмную визуализацию кровотока в сосудах.
- Дуплексное ультразвуковое сканирование – позволяет определить количество поражённых сосудов.
- Магнитно-резонансная ангиография – распознаёт функциональные особенности сосудов и их анатомические изменения.
Венозная мальформация вен нижних конечностей требует незамедлительных мер по лечению. Запущенная венозная мальформация вен приводит к серьёзным последствиям, которые угрожают жизни пациента.
Как и где получить лечение венозной мальформации вен на ногах
Если вы наблюдаете у себя на коже фиолетовые, розовые и красные пятна или у вас уже диагностирована венозная мальформация вен на ногах — запишитесь на консультацию в Сосудистый центр в Москве по телефону +7 (499) 464-03-03. Наши специалисты проводят диагностику и лечение ангиодисплазий различной степени развития.
Мы находимся по адресу: г. Москва, Гагаринский переулок, д. 37/8 (метро «Смоленская» Арбатско-Покровской линии, метро «Кропоткинская»). Любой вопрос, связанный с работой Флебологического центра можно задать по электронной почте info@vascul.ru.
Не откладывайте лечение на «потом», обратитесь в Сосудистый центр сейчас, чтобы обезопасить себя от негативных последствий заболевания в будущем.
Проявления аномалий венозных сосудов
Симптоматика аномалий венозного русла мозга проявляется при рождении уже у половины малышей. Главный признак аневризматического изменения вены Галена — недостаточность сердца, связанная с повышенным венозным давлением в мозговых и полой вене, создающим избыточную нагрузку на сердце ребенка. Поскольку аневризма функционирует во время внутриутробного периода, к моменту рождения у малыша формируется высокая вероятность декомпенсации сердечной деятельности.
ребенок с диагностированной мальформацией вены Галена
Клиническими признаками аневризмы считаются:
- Быстрая утомляемость ребенка во время кормления;
- Отеки мягких тканей;
- Одышка с риском отека легких;
- Отставание физического развития с первых месяцев жизни.
Неблагоприятным признаком нарушенного венозного оттока является гидроцефальный синдром, который говорит о сдавлении из вне расширенными сосудами водопровода мозга, несущего ликвор от боковых желудочков и субарахноидальных пространств, или о сильном сбросе большого количества крови в вены черепа.
Клиническая картина и симптоматика артериовенозных мальформаций сосудов головного мозга (АВМ)
Наиболее часто артериовенозная мальформация проявляют себя:
- Кровоизлиянием;
- Эписиндромом;
- Очаговой неврологической симптоматикой;
- Общемозговой симптоматикой.
Риск кровоизлияния из АВМ ежегодно составляет 2-4% и в отличие от артериальных аневризм риск кровоизлияния со временем только возрастает. Считается что наиболее часто разрываются небольшие по размеру АВМ (так как скорость кровотока в них выше). После уже состоявшегося кровоизлияния риск повторного кровотечения только возрастает и составляет ежегодно 10-15%.
Клиническое значение имеют размеры гематомы и ее локализация. Наиболее опасны гематомы ствола головного мозга, гематомы в задней черепной ямке, в IV желудочке. Большие гематомы опаснее маленьких.
Очень часто встречаются сочетания артериальной аневризмы и артериовенозных мальформаций, причем аневризма может быть нодальная, т. е. в толще тела АВМ (в клубке) и экстранодальная — локализоваться, например, на афферентном артериальном сосуде.
Эписиндром. Вторая по частоте разновидность проявления АВМ. Судороги могут носить всевозможные формы. Наиболее эпилептогенны АВМ в области медиальных отделов височных долей головного мозга, полюсов лобных долей. АВМ вызывает выраженные атрофические изменения прилежащего мозгового вещества (за счет синдрома обкрадывания), зачастую с наложениями гемосидерина, что приводит к развитию патологической электрической активности.
Очаговая симптоматика. Зависит от топического расположения артериовенозной мальформации и может проявляться парезами, параличами, чувствительными расстройствами и т.д.
Общемозговая симптоматика — головная боль так же очень характерна и может носить распирающий характер, пульсирующий, с шумом в голове.
Гигантские АВМ могут оказывать влияние на системную гемодинамику, изменяя объемные показатели работы сердца.
Принципы микрохирургического удаления АВМ
|
АВМ. Вид на операции |
Прямые хирургические вмешательства предпочтительно проводить в холодном периоде после кровоизлияния, так как сопутствующие изменения мозга затрудняют выделение АВМ, что приводит к усугублению травмы мозга и тяжелее переносятся больным. В остром периоде паренхиматозного кровоизлияния оправдана тактика удаления больших гематом без попыток иссечения АВМ. Операция по одномоментному удалению гематомы и мальформации может быть выполнена при небольших лобарных АВМ. Следует помнить, что в условиях наличия гематомы и отека мозга, контрастирование АВМ может существенно отличаться от истинного вследствие компрессии сосудов мальформации. При глубинных АВМ, а также при АВМ больших размеров, целесообразно дождаться рассасывания гематомы. В случае вентрикулярного кровоизлияния показана установка наружного вентрикулярного дренажа. Трепанация должна быть выполнена таким образом, чтобы, помимо узла АВМ, обеспечить визуализацию афферентных артерий и основных дренажных вен мальформации на протяжении
При выделении питающих сосудов АВМ, для меньшей травматизации мозгового вещества важно использовать естественные борозды и пространства (например: широкая препаровка латеральной щели при выделении афферентов, идущих от средней мозговой артерии; межполушарные доступы для контроля афферентов, идущих от перикаллезной или задней мозговой артерий и т. п.)
Выключение афферентных артерий необходимо производить на минимальном отдалении от клубка АВМ. Это связано с тем, что от питающих АВМ артерий, могут отходить ветви к мозговой паренхиме. Данное положение особенно актуально при иссечении АВМ глубинной и парастволовой локализации, когда могут пострадать ветви, кровоснабжающие функционально важные структуры. Во избежание травмы сосудов АВМ ее выделение должно осуществляться единым блоком по перифокальной зоне. У больных после кровоизлияния один из полюсов клубка АВМ может быть четко отграничен от мозга внутримозговой гематомой или постгеморрагической кистой, что упрощает хирургические манипуляции. Следует помнить, что в ряде случаев гематома может фрагментировать АВМ, в связи с чем ревизия стенок полости удаленной АВМ обязательна. Пересечение основных дренажных вен должно проводиться после полного выделения АВМ. Принцип поэтапного выключения артериального притока по мере выделения клубка, а венозного — по завершении диссекции АВМ, хорошо известен. При сокращении венозного дренирования в условиях сохраняющегося артериального притока узел АВМ становиться напряженным и кровоточивым. В определенных случаях при дисбалансе кровотока происходят самопроизвольные разрывы тонких сосудов мальформации, ведущие к интенсивному кровотечению, которое крайне сложно остановить. Единственным выходом в такой ситуации является быстрое выделение АВМ с выключением афферентов. Поскольку стенки артерий мальформации в отличие от нормальных сосудов имеют истонченный мышечный слой, коагулировать сосуды необходимо тщательно и на протяжении. К значимым интраоперационным осложнениям следует отнести воздушную эмболию. В послеоперационном периоде ухудшение в неврологическом статусе отмечено у 30% больных при значительном регрессе выраженности симптоматики в большинстве случаев. Послеоперационная летальность составила 1,3%. Послеоперационные зрительные расстройства являются достаточно стойкими и практически не регрессируют. При речевых послеоперационных нарушениях в подавляющем большинстве случаев удается добиться значительного регресса симптоматики, а у многих больных полностью избавится от дефекта речи.
Уход
Лечение зависит от анатомии порока развития, определяемой с помощью ангиографии или магнитно-резонансной томографии (МРТ).
Хирургический
Следует регулярно измерять окружность головы и тщательно контролировать ее для выявления гидроцефалии
Важное значение имеют нейрохирургические процедуры для снятия гидроцефалии. Вентрикулоперитонеальный шунт может потребоваться в некоторых младенцев
Для лечения тяжелой недостаточности, если таковая имеется, следует проконсультироваться с детским кардиологом. Часто пациенты нуждаются в интубации. В большинстве случаев свищевые артерии, впадающие в Вену Галена, необходимо блокировать, тем самым уменьшая кровоток в вену. Открытая хирургия отличается высокой заболеваемостью и летальностью. Последние достижения последних нескольких десятилетий сделали эндоваскулярную эмболизацию предпочтительным методом лечения. Эти методы лечения предпочтительны, поскольку они не представляют серьезной угрозы для окружающей мозговой ткани. Однако было зарегистрировано несколько случаев рецидива артериовенозных мальформаций. Молодой возраст многих пациентов, сложная анатомия сосудов и чувствительное расположение вены Галена создают серьезные проблемы для хирургов. Другой вариант лечения — лучевая терапия. Лучевая терапия , также называемая радиохирургией , включает использование сфокусированных лучей для повреждения кровеносных сосудов. Лучевая терапия часто не используется в качестве лечения, потому что эффект от процедуры может длиться месяцами или годами, и существует риск повреждения прилегающих тканей головного мозга.
Медицинская помощь
Хирургическое вмешательство не всегда возможно, когда анатомия мальформации создает слишком большой риск. Благодаря недавним улучшениям в эндоваскулярных процедурах многие случаи, которые не были доступны хирургическим путем, стали поддающимися лечению. Эндоваскулярное лечение включает доставку лекарств, баллонов или спиралей к месту уродства через кровеносные сосуды через катетеры. Эти методы лечения работают за счет ограничения кровотока по венам. Однако риск осложнений от эндоваскулярного лечения все еще существует. Стенка вены может быть повреждена во время процедуры, а в некоторых случаях эмболы могут смещаться и перемещаться по сосудистой системе. Для оценки одного плода и пяти новорожденных с мальформацией вены Галена использовалась двумерная эхокардиография с цветными изображениями и импульсным ультразвуковым допплером. Цветная визуализация и импульсная допплеровская ультрасонография предоставили анатомическую и патофизиологическую информацию, касающуюся сердечной гемодинамики и внутричерепного кровотока; с учетом клинического состояния пациента эти методы предоставили надежные неинвазивные средства для оценки эффективности терапии и необходимости дальнейшего лечения новорожденных с пороками развития вены Галена. Когда ни одна из этих процедур неэффективна, можно использовать шунтирование для уменьшения давления внутри варикозного расширения вен . При припадках обычно используются противоэпилептические препараты.
Диагностика
Исследование на наличие уродливой вены Галена показано, когда у пациента сердечная недостаточность, не имеющая очевидной причины. Диагноз обычно устанавливается по таким признакам, как черепно-мозговые ушибы, и по таким симптомам, как расширение лицевых вен. Вену Галена можно визуализировать с помощью ультразвука или . Деформированная большая мозговая вена будет заметно увеличена. Ультразвук — особенно полезный инструмент при пороках развития вены Галена, потому что очень много случаев происходит в младенчестве, а ультразвуковое исследование может поставить диагноз в пренатальном периоде. Многие случаи диагностируются только при вскрытии, поскольку застойная сердечная недостаточность возникает очень рано.
Классификация
Описаны пять типов галеновых артериовенозных мальформаций:
| Схема 1 | Многие сосуды, включая передние церебральные артерии, перфорирующие таламические артерии и верхние мозжечковые артерии, выходят в вену Галена. |
|---|---|
| Схема 2 | Единственная задняя сосудистая артерия впадает в вену Галена. |
| Схема 3 | Одна или обе задние сосудистые артерии и одна или обе передние мозговые артерии впадают непосредственно в систему Галена. |
| Схема 4 | Ангиоматозная сеть задней хориоидальной и таламической перфорирующих артерий напрямую входит в Вену Галена. |
| Схема 5 | Артериовенозная мальформация с высоким потоком в правой нижней лобной доле дренируется через нижний сагиттальный синус и периклозальную вену в вену Галена. |
Эти пороки развития развиваются внутриутробно из-за наличия свищей между примитивными мягкими паутинными артериями и пиальными венами, пересекающими друг друга под прямым углом. Поскольку примитивная система Галена и примитивная хориоидальная система лежат близко друг к другу, артериовенозная мальформация, вовлекающая примитивную хориоидальную систему, неизбежно затронет Галеновую вену. Более крупные артериовенозные шунты коррелируют с более сильными гемодинамическими эффектами и более ранним проявлением симптомов; небольшие артериовенозные шунты коррелируют с более сильным локальным массовым эффектом, вызывая прогрессирующее неврологическое нарушение.
Дуплексная допплеровская ультрасонография
Ультрасонография является безопасным, недорогим и эффективным методом диагностики ПГ. Узловая структура печени, спленомегалия и наличие коллатеральной циркуляции позволяют заподозрить цирроз печени и ПГ. Определяется также диаметр спланхнических сосудов, направление и скорость кровотока, изменения диаметра сосудов при дыхании, индекс портального венозного застоя, пульсаторный индекс, индекс резистентности печеночной, верхней брыжеечной и селезеночной артерий и печеночный сосудистый индекс. В норме диаметр воротной вены не превышает 13 мм при спокойном дыхании, при глубоком он может увеличиваться на 50%. Расширение констатируется при диаметре вены >15 мм во время спокойного дыхания. При повышении давления кровоток в воротной вене замедляется и становится монотонным (без дыхательных колебаний) и, в конце концов, полностью ретроградным, направленным в сторону функционирующих портокавальных шунтов.
Однако воспроизводимость и точность количественных ультразвуковых параметров недостаточная, они зависят как от техники исследования, так и от суточных ритмов, состояния симпатической нервной системы, принятых медикаментов и тому подобное. Так, например, диаметр воротной вены (одновременно с нижней полой веной) может увеличиваться при длительной застойной сердечной недостаточности. Поэтому применение дуплексной допплеровской ультрасонографии самой по себе не рекомендуется для установления точного диагноза ПГ, неясным остается ее диагностическое значение на ранних стадиях ПГ (в большинстве таких исследований участвовали пациенты с тяжелым циррозом и выраженной ПГ). Тем не менее данный метод является ценным при первичном обследовании, он также помогает установить причины ПГ, например, обструкцию сосудов на различных уровнях. Метод также высокочувствителен относительно выявления функционирующих портокавальных анастомозов. После наложения TIPS или портокавальных анастомозов допплеровская ультрасонография играет большую роль в контроле проходимости шунта.
Компьютерная томография используется как качественный (не количественный) метод диагностики, если ультрасонография не дала четких результатов. В отличие от ультрасонографии, на результаты КТ не влияет наличие газа в кишечнике. Реконструкция анатомии сосудистой сети при помощи 3-D технологии позволяет точно воспроизвести структуру портальной венозной системы и коллатералей. Частой находкой на КТ при портальной гипертензии является дилатация нижней полой вены. Однако КТ не позволяет оценить кровоток по венозным и артериальным сосудам. МЯР дает возможность, помимо качественной, получить также и количественную информацию, например, оценить венозный поток по воротной и непарной венам. Тем не менее, проведение МЯР не исключает необходимости инвазивных исследований.
В случаях сомнений относительно причин поражения печени целесообразной может стать пункционная биопсия: некроз третьей зоны, например, свидетельствует о портальной гипертензии, вторичной по отношению к сердечной недостаточности, а нормальная паренхима печени — о подпеченочных причинах ПГ. Противопоказанием для биопсии печени является коагулопатия и выраженный асцит.
Виды церебральных мальформаций венозно-артериального русла
Патологические образования принято различать по топографо-анатомическому признаку, гемодинамической активности, размерам. Первый параметр характеризует место расположения мальформации в головном мозге, отсюда происходят их названия:
- поверхностные АВМ – сосредоточены в коре больших полушарий мозга (на поверхности мозга) и прилежащих структурах белого вещества;
- глубинные АВМ – локализуются в глубине мозговых извилин, базальных ганглиях, внутри желудочков, в структурах ствола ГМ.
По гемодинамической активности выделяют мальформации:
- активные – к ним причисляют смешанного вида АВМ ГМ (самая частая разновидность, при которой обнаруживается частичная деструкция капилляров) и фистулезного типа (артерия прямо переходит в вену, капиллярная сеть полностью разрушена);
- неактивные – капиллярные (телеангиоэктазии), венозные, артериовенозные кавернозные.
Поражение также оценивается по размерам, учитывается диаметр только клубка мальформации. При диагностике размеров используют следующие наименования АВМ:
- микромальформации – менее 10 мм;
- малые – от 10 мм до 20 мм;
- средние – 20-40 мм
- большие – 40-60 мм
- гигантские – более 6 см в диаметре.
Для предупреждения тяжелой геморрагии и связанных с ней необратимых осложнений крайне важно выявить и устранить очаг в ближайшее время, до разрыва. Почему? Объяснение куда более убедительное –при разрывах слишком большой процент людей погибает (до 75% пациентов) от обширного кровоизлияния, несопоставимого с жизнью
Необходимо понимать, что сосуды АВМ слишком подвержены прорывам, так как они серьезно истощены на почве ненормального строения и нарушенного тока крови. Одновременно с этим, крупные порочные образования сдавливают и повреждают окружающие мозговые ткани, что несет дополнительную угрозу состоятельности функций ЦНС. Поэтому, если диагноз подтвержден клинически, оттягивать с лечением ни в коем случае нельзя.
Заключение
Оптимальным методом лечения АВМ следует считать мультимодальный подход с использованием комбинаций всех методов. Микрохирургическое иссечение в настоящее время остается основным радикальным методом лечения АВМ головного мозга. Благодаря дифференцированному подходу по отбору пациентов в большинстве случаев удается достичь благоприятных результатов. Эмболизация имеет существенное значение в структуре комбинированных методов лечения. Метод высокоэффективен при лечении фистульных АВМ и АВМ вены Галена мурального типа. Лучевая терапия — метод выбора при распространенных и неоперабельных АВМ, а также при частичном иссечении или неполной облитерации АВМ после ее эндоваскулярной эмболизации.