Функциональная кардиопатия
Содержание:
Виды
Кардиомиопатия бывает:
- первичная,
- вторичная.
Первичная возникает под действием вирусного заражения организма, аутоиммунных заболеваний, разрастания соединительной ткани с одновременным формированием рубцов. Причиной первичной формы могут быть также и изменения в геноме, вызвавшие нарушение в строении любого из белков, участвующих в метаболизме сердечных клеток.
- эндокринных,
- сосудистой,
- инфекционных.
Кроме первичной и вторичной в кардиологии выделяют несколько видов кардиомиопатий по механизму развития:
- гипертрофические,
- алкогольная кардиомиопатия,
- с развитием дилатации,
- гормональные,
- рестриктивные.
Причины кардиомиопатии
Кардиомиопатия развивается по нескольким причинам. Специалисты делят их на группы
- врожденные,
- воздействия на организм в течение жизни,
- смешанные.
Врожденная кардиомиопатия формируется из-за сбоев в закладке сердечных тканей во время развития зародыша. Появление нарушений в эмбриогенезе провоцируют вредные привычки будущей мамы, перенесенные ею стрессы, неправильное питание.
Кардиомиопатия, развившаяся в течение жизни как результат другого заболевания, формируется из-за нарушения обмена в сердечных тканях, скопления в них ядовитых веществ или патологических включений (жидкостей). Привести к появлению дефектов в миокарде может длительная диета с исключением мясных продуктов или долгое голодание.
Кардиомиопатия. Симптомы
Степень проявления заболевания зависят от множества факторов. На выраженность симптомов влияют:
- степень разрушения миокарда,
- артериальное давление,
- недостаточность в работе клапанов,
- уменьшение левого желудочка.
В начальной стадии жалобы у больных на сердечные боли отсутствуют. В запущенных случаях больной может чувствовать одышку, боль в грудной клетке, Сердцебиение. При тяжелой форме к дискомфорту в груди и одышке присоединяются отеки на ногах и посинение кончиков пальцев.
Кардиомиопатия. Методы диагностики
При каких симптомах следует поспешить к кардиологу:
- в сердце появились боли неснимаемые нитроглицерином,
- начались перебои в работе сердца,
- сердцебиение учащается или замедляется,
- появились головокружения,
- незначительная физическая активность приводит к сильной одышке,
- с каждым месяцем отеки на ногах становятся все больше,
- кожа бледная или синеватая,
- увеличились печень и селезенка.
Перечисленные признаки говорят о развивающейся сердечной недостаточности. Несколько таких симптомов должны заставить немедленно посетить квалифицированного кардиолога и пройти мероприятия по диагностике.
Способы диагностики:
- ЭКГ,
- мониторинг сердца и давления,
- УЗИ сердца и сосудов,
- исследование крови.
Врач может назначить и дополнительные исследования, не вошедшие в список. Они необязательны, но в некоторых случаях помогают уточнить диагноз.
Диагноз “кардиомиопатия” ставят, когда заболевание сердца обнаружено, но диагностические мероприятия показали, что патология возникла не вследствие врожденных аномалий, воспалений, или опухолей. Таким образом, чтобы поставить диагноз «кардиомиопатия» врачу приходится последовательно исключать ряд распространенных сердечных заболеваний.
Методы лечения кордиомиопатии
При первичной форме болезни назначается симптоматическое лечение. Терапия должна быть направлена на устранение боли в сердце, одышки, нарушения кровообращения.
Усилия врачей при лечении кардиопатии направлены на создание условий, уменьшающих нагрузку на сердце, чтобы прекратить развитие сердечной недостаточности. Пациенту выписывает лекарства для внутреннего применения. Их наименование и дозировка подбираются индивидуально в зависимости от тяжести заболевания и клинической картины.
Обратимая кардиомиопатия развивается сразу после родов или в последний триместр из-за адаптации системы кровообращения к изменениям в организме. В некоторых случаях назначается курс поддерживающей терапии, но чаще патология со временем исчезает сама.
Прогноз заболевания зависит степени его развития и адекватности назначенной терапии. В неблагоприятном случае сердечная недостаточность будет прогрессировать, состояние пациента ухудшаться.
В современных клиниках используют последние достижения кардиологии. Опытные врачи регулярно проходят переаттестацию, участвуют в семинарах и конференциях, обмениваясь опытом
Кардиомиопатия находится под пристальным вниманием кардиологов. С каждым годом появляются новые разработки, позволяющие проводить лечение более эффективно
Поэтому если вам поставили этот диагноз не стоит отчаиваться. При правильном лечении прогноз будет благоприятным.
ПРОСМОТРОВ:
662
Таурин
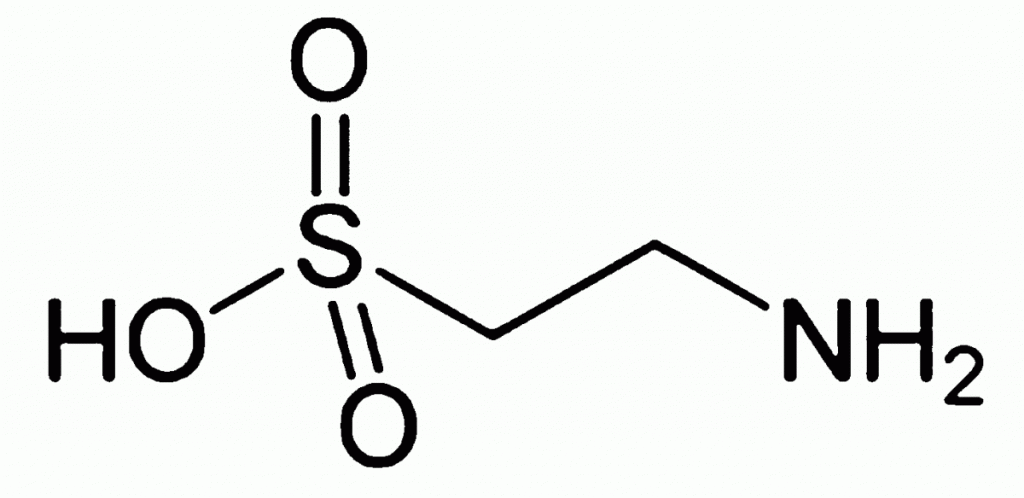
Таурин — сульфокислота, образующаяся в организме из аминокислоты цистеина. Относится к группе сенситайзеров — веществ, повышающих чувствительность периферических тканей к инсулину.
|
Сенситайзеры — повышают чувствительность периферическихтканей и органов-мишеней к инсулину. Сенситайзеры включают в себя: бигуаниды – метформин (Сиофор, Глюкофаж); тиазолидиндионы (глитазоны): пиоглитазон (Актос, Диабнорм), росиглитазон (Авандия, Роглит). Место действия – гепатоциты, мышечная и жировая ткани. Улучшают периферическую утилизацию глюкозы, но не оказывают стимулирующего действия на бета-клетки поджелудочной железы. Поэтому они не повышают уровень инсулина в крови и не вызывают гипогликемических состояний (то есть не снижают содержание глюкозы в крови ниже нормального уровня) . |
Таурин, являясь естественным продуктом обмена серосодержащих аминокислот, обладает многообразными метаболическими эффектами, в том числе влияет на кальцийзависимые процессы в клетке и на протеинкиназу С, а через эти механизмы оказывает модулирующее влияние на метаболизм углеводов.
У взрослого человека весом 70 кг содержится около 70 г таурина. У больных сахарным диабетом концентрация таурина снижена, падает концентрация таурина у пожилых людей по отношению к молодым почти в два раза, при травме таурин теряется значительно. Уровень таурина необходимо восстанавливать. Известно, что недостаток его может приводить к кардиопатии, ретинопатии и др. последствиям. При гестационном сахарном диабете уровень таурина в крови женщин понижен. Таурин, по всей видимости, является ярким маркером измененного метаболизма глюкозы во время беременности у женщин с гестационным диабетом.
Если говорить о клинической стороне действия таурина, то он благоприятно воздействует на гемостаз: на агрегацию тромбоцитов и эритроцитов, проявляет защитные свойства при невропатии, кардиомиопатии, нефропатии и ретинопатии, защищает бетаклетки при гипергликемии от повреждающего действия супероксида. Недавние исследования показали роль таурина в развитии плода, а также в подавлении развития толерантности к глюкозе у ребенка, рожденного от диабетической матери.
Не является неожиданным влияние Дибикора на липидный обмен. Участие таурина в метаболизме жиров также известно очень давно. Входя в состав желчных кислот, таурин участвует в дисмульгации и во всасывании жирорастворимых соединений, в том числе и витаминов.
При преимущественном потреблении глицина или таурина с пищей происходит изменение образования в сторону гликохолевой (G) или таурохолевой (T) кислоты. Так, например, если человеку добавлять таурин, соотношение G/T уменьшается. Надо отметить, что свойства кислот не совсем идентичны. При всех равных условиях в печени человека синтез идет с предпочтением таурохолевых кислот. При потреблении таурина значительно увеличивается скорость экскреции желчных кислот и их объем. Глицин не обладает таким эффектом. Таким образом, при недостаточности таурина будет страдать выделение желчных кислот. В эксперименте обнаружено, что на холестериновой диете образование холестериновых камней в желчном пузыре достигает 71-100% при дефиците таурина, не происходит образование камней при добавлении в рацион таурина
Рекомендованные дозы при гиперинсулинемии — 1000 мг (500 мг 2 раза в день) в сутки за полчаса до еды. Таурин может повысить индекс массы тела, так как жировая ткань (впрочем, как и мышечная) является инсулинзависимой зоной .
Среди БАДов для улучшения качества волос таурин присутствует в препарате «Иннеов густота волос» (75 мг).
Причины СССУ
Первичная дисфункция:
- Замещение клеток соединительной тканью — кардиосклероз (постинфарктный, постмиокардитический, кардиомиопатический).
- Врожденное недоразвитие синусового узла.
- Старческий амилоидоз.
- Идиопатическое повреждение, в том числе болезнь Ленегра.
Вторичная дисфункция:
- Повышение тонуса вагуса (блуждающего нерва): синдром каротидного синуса, апноэ сна, вазовагальный обморок, увеличение внутричерепного давления, инфаркт миокарда нижней топики, субарахноидальное кровоизлияние, рефлекс Бецольда–Яриша, болезни гортани и пищевода, кардиоверсия.
- Воздействие лекарств: бетаадреноблокаторы, недигидропиридиновые блокаторы кальциевых каналов, сердечные гликозиды, антиаритмики, холиномиметики, морфин, тиопентал натрия, препараты лития.
- Воспаление сердечной мышцы (миокардит).
- Ишемизация синусового узла.
- Острое повреждение СУ при инфаркте правого предсердия
- Травматическое повреждение клеток синусового узла, проводящей системы (операция, ранение).
- Электролитные нарушения.
- Нарушения газового состава крови (гипоксемия, гиперкапния).
- Дисфункция гормональных систем (чаще всего гипотиреоз).
Патологическая анатомия
При морфологическом исследовании сердца вовлеченным оказывается чаще ПЖ, который имеет пятнистый вид: измененные участки могут быть окружены нормальными тканями. Вовлечение ПЖ может быть регионарным (20%) или диффузным (80%). Миокард ПЖ прогрессивно редуцируется, замещаясь жировой и фиброзной тканью, которая отличается от нефиброзной жировой инфильтрации, возникающей в ПЖ с возрастом. На ранних стадиях заболевания стенки правых отделов сердца утолщаются, но в дальнейшем из-за накопления жировой ткани и появления участков дилатации они становятся более тонкими (рис. 12.1а, б).
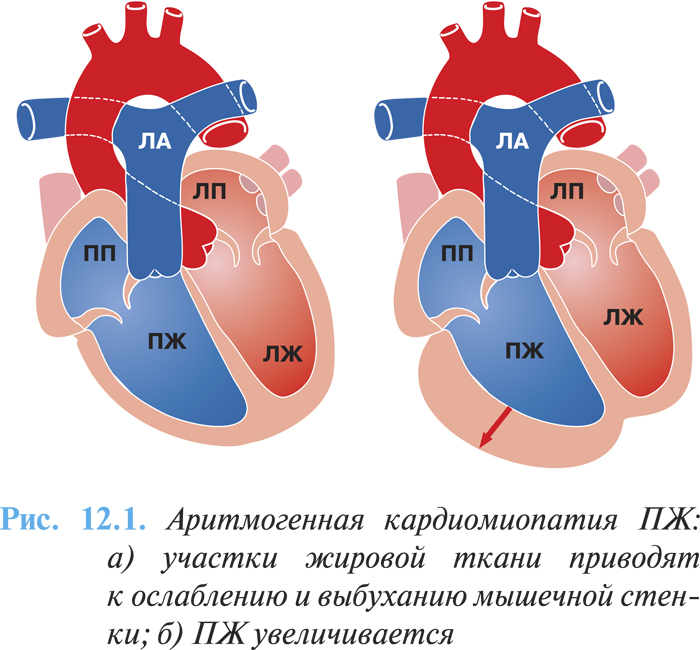
Жировое перерождение миокарда распространяется чаще от эпикардиальных слоев к эндокарду. Миокард поражается преимущественно в области выносящего тракта, верхушки и субтрикуспидальной зоны, которые рассматриваются в качестве «треугольника дисплазии».
При аритмогенной кардиомиопатии ПЖ липоматоз сопровождается преимущественно дилатацией выносящего тракта ПЖ или генерализованной дилатацией. Фибролипоматоз характеризуется наличием фокальной аневризмы ПЖ и выпячиванием в области верхушки, нижней стенки, субтрикуспидальной и инфундибулярной зоны.
По мере прогрессирования фиброзно-жировая дистрофия поражает также ЛЖ и предсердия.
ТЕРМИНОЛОГИЯ И ОПРЕДЕЛЕНИЯ
Краткая информация о терминологии, которая используется при этой эхокардиографической технике и описанная в тексте, приведена в Таблице 1.
Таблица 1. Speckle-tracking эхокардиографическая терминология
Напряжение Strain — Деформации миокарда
Скорость деформации Strain rate — Скорость деформации миокарда
Продольная деформация Longitudinal strain — Миокардиальная деформация, направленная от основания к верхушке сердца
Радиальная деформация Radial strain — Деформации миокарда, направленная радиально к центру полости левого желудочка
Циркулярная деформации Circumferential strain — Сокращение левого желудочка вдоль циркулярного периметра, наблюдаемое в плоскости короткой оси
Скручивание Twisting — Чистая разница между средним верхушечным и базальным вращением в фазе систолы
Кручение (торсия) Torsion — Скручивание ЛЖ нормализованное к расстоянию основание-верхушка
Раскручивание Untwisting — Чистая разница между средним верхушечным и базальным вращением в фазе диастолы
Частота раскручивания — Untwisting rate Скорость раскручивания
Bull’s-eye (Мишень) — Значение деформации топографического изображения для всех 17 сегментов
Постсистолический индекс Post-systolic index — Процент от значения постсистолической деформации по сравнению с максимальным пиком деформации
Лечение
Для выбора антиаритмической терапии необходимо проведение инвазивного ЭФИ и проб с дозированной физической нагрузкой.
Среди антиаритмических препаратов эффективны амиодарон и соталол. Дигоксин применяют при тахисистолической форме фибрилляции предсердий для замедления ЧСС. Для восстановления синусового ритма проводят кардиоверсию.
Диуретики применяют при СН у больных с задержкой жидкости.
Из хирургических методов лечения применяют абляцию, если источник нарушенной электрической активности идентифицирован с помощью электрофизиологических тестов. В случаях если аритмии не контролируются с помощью лекарственных средств или абляции (обширное поражение или наличие множественных аритмогенных очагов), вшивают имплантируемый кардиовертерный дефибриллятор, в некоторых случаях требуется имплантация водителя ритма. Трансплантацию сердца применяют редко, если контроль ритма невозможен другими методами.
12.2. ГИПЕРТРОФИЧЕСКАЯ КАРДИОМИОПАТИЯ
Гипертрофическая кардиомиопатия — достаточно распространённое поражение сердца генетической природы, характеризующееся утолщением стенок левого желудочка. Гипертрофия стенки левого желудочка более 15 мм неясного генеза считается диагностическим критерием гипертрофической кардиомиопатии.
Различают обструктивную (сужающую выносящий тракт левого желудочка) и необструктивную гипертрофические кардиомиопатии. Гипертрофия может быть симметричной (увеличение с вовлечением всех стенок левого желудочка) и асимметричной (увеличение с вовлечением одной из стенок). Гипертрофия может охватывать изолированно лишь верхушку сердца (апикальная гипертрофическая кардиомиопатия). При гипертрофии верхней части межжелудочковой перегородки непосредственно под фиброзным кольцом аортального клапана говорят о мышечном субаортальном стенозе.
Важными общими особенностями гипертрофической кардиомиопатии (как с обструкцией, так и без неё) выступают высокая частота нарушений ритма сердца, прежде всего желудочковой экстрасистолии и пароксизмальной тахикардии. С аритмиями связывают внезапную смерть, наступающую у 50% больных гипертрофической кардиомиопатией.
Эпидемиология
Гипертрофическую кардиомиопатию наблюдают у 0,2% населения, чаще в виде необструктивных форм (70-80%), реже — обструктивных (20-30%, в виде идиопатического гипертрофического мышечного субаортального стеноза). Заболеваемость у детей составляет 0,3-0,5 случаев на 100 000 населения. Нередко болезнь развивается в зрелом и пожилом возрасте, хотя в последнем случае диагностика заболевания может вызвать трудности, поскольку возможна связь заболевания с атеросклеротическим поражением. Мужчины болеют чаще женщин. Возможно сочетание болезни с другой патологией генетической природы.
ЭТИОЛОГИЯ
Гипертрофическую кардиомиопатию считают наследственным заболеванием. Она наследуется аутосомно-доминантным путём в результате мутаций одного из следующих генов кодирующих белки саркомера:
• β-тяжёлая цепь миозина, ген локализован в хромосоме 14;
• тропонин T сердечной ткани, ген в хромосоме 1;
• тропомиозин, ген в хромосоме 15;
• миозин-связывающий белок C, ген в хромосоме 11;
• лёгкие цепи миозина (хромосомы 3 и 12);
• актин (хромосома 15), титин, тропонин C.
Семейный характер патологии отмечают более чем у половины больных. При этом в одной семье имеются признаки одной и той же мутации. Выявлены по крайней мере 10 генетических локусов, ответственных за возникновение заболевания. В этих генах обнаружено более 100 мутаций, вызывающих гипертрофическую кардиомиопатию. Выживаемость больных гипертрофической кардиомиопатией, возникшей в результате особо клинически злокачественной мутации гена β-тяжёлой цепи миозина, существенно ниже, чем при мутации гена сердечного тропонина T, причём в последнем случае клинические проявления возникают в более позднем возрасте. Генетические исследования показывают, что у близких родственников больных нередко имеются те же генетические мутации, однако без неблагоприятных фенотипических признаков (здоровые носители мутировавщего гена). У этих лиц гипертрофия миокарда может развиться спустя много лет.
ПАТОГЕНЕЗ
Большинство мутаций генов саркомеров приводят к замене одной аминокислоты в белке, имеющем важное функциональное значение. В результате мутации генов возникает гипертрофия левого желудочка и участки дезорганизации кардиомиоцитов
Механизмы, приводящие к характерным изменениям, остаются неясными.
Что такое дилатационная кардиомиопатия?
Дилатационная кардиомиопатия (ДКМП) представляет собой состояние, при котором способность сердца качать кровь снижается из-за увеличения и ослабления левого желудочка, главной насосной камеры сердца. Зачастую это не позволяет сердцу наполниться кровью, как следует. Со временем это может повлиять также на другие камеры сердца.
Симптомы дилатационной кардиомиопатии
Многие люди с ДКМП не имеют либо никаких признаков болезни, либо только незначительные симптомы, и живут абсолютно нормальной жизнью. У других же пациентов симптомы могут прогрессировать и обостряться, ухудшая тем самым работу сердца.
Симптомы дилатационной кардиомиопатии могут возникнуть в любом возрасте и включают в себя:
- симптомы сердечной недостаточности (одышка и усталость)
- отек нижних конечностей
- усталость (чувство чрезмерной усталости)
- прибавка в весе
- обморок, возникающий в связи с нерегулярными сердечными ритмами, неправильной работой кровеносных сосудов, или вовсе без какой либо причины
- учащенное сердцебиение (из-за нарушения сердечного ритма)
- головокружение — при дилатационной кардиомиопатии образуются сгустки крови из-за которых кровь течет медленнее. Если этот кровяной сгусток отрывается, он может достичь легкие (легочная эмболия), почки (почечная эмболия), головной мозг (мозговая эмболия или инсульт) или конечности (периферическая эмболия)
- боль или давление в груди(происходит обычно при физической нагрузке на организм, но также может произойти во время отдыха или после еды).
Причины дилатационной кардиомиопатии
Дилатационная кардиомиопатия может быть унаследована (семейная ДКМП), но в первую очередь эта болезнь сердца может быть вызвана рядом других факторов, в их числе:
- тяжелое заболевание коронарной артерии
- алкоголизм
- заболевания щитовидной железы
- диабет
- вирусные инфекции сердца
- аномалии клапанов сердца
- прием наркотиков
- ДКМП также может возникнуть у женщин после родов (послеродовая кардиомиопатии).
Офлайн анализ
Записанные данные обрабатываются с помощью специфического acoustic-tracking программного обеспечения, как правило, доступного на специальных рабочих станциях, что позволяет выполнять автономный (после обследования) полуавтоматический анализ деформации на основе спеклов. Анализируемая поверхность эндокарда миокардиальных сегментов, определяется вручную у верхушки и / или в плоскости короткой оси сердца с помощью подхода «указал и щёлкнул, point-and-click». Поверхность эпикарда помечается, а затем автоматически генерируется системой, создавая тем самым поле зрения. После ручной настройки ширины и формы поля зрения, программное обеспечение автоматически делит поле зрения на 6 сегментов, и в результате автоматически подсчитывается качество трекинга (tracking) для каждого сегмента и, либо применяется либо отвергается, с возможностью дальнейшей ручной коррекции. Сегменты, для которых нет возможности получения адекватного качественного изображения, отклоняются программным обеспечением и исключаются из анализа. Последнее: когда поле зрения оптимизировано, программное обеспечение генерирует кривые деформации для каждого выбранного миокардиального сегмента (Рис. 1). Из этих кривых, исследователь может получить значения регионального и глобального (путем усреднения значений, наблюдавшихся во всех сегментах) пиков и времени достижения пика.
Если продольный анализ деформации выполняется во всех 3 апикальных плоскостях, программное обеспечение автоматически генерирует топографическое представление всех 17 проанализированных сегментов (bull’s eye ― мишень; Рис. 3А). С помощью простого ввода оператор может также получить параметры времени достижения пика продольной деформации и постсистолический индекс (например, процент постсистолического значения деформации по сравнению с максимальным пиком деформации оцениваемого сегмента) bull’s eye ― мишень (Рис. 3В), которые оказались полезными в предварительных исследованиях для анализа и выявления потенциальной ишемии или зон миокардиальной диссинхронии.
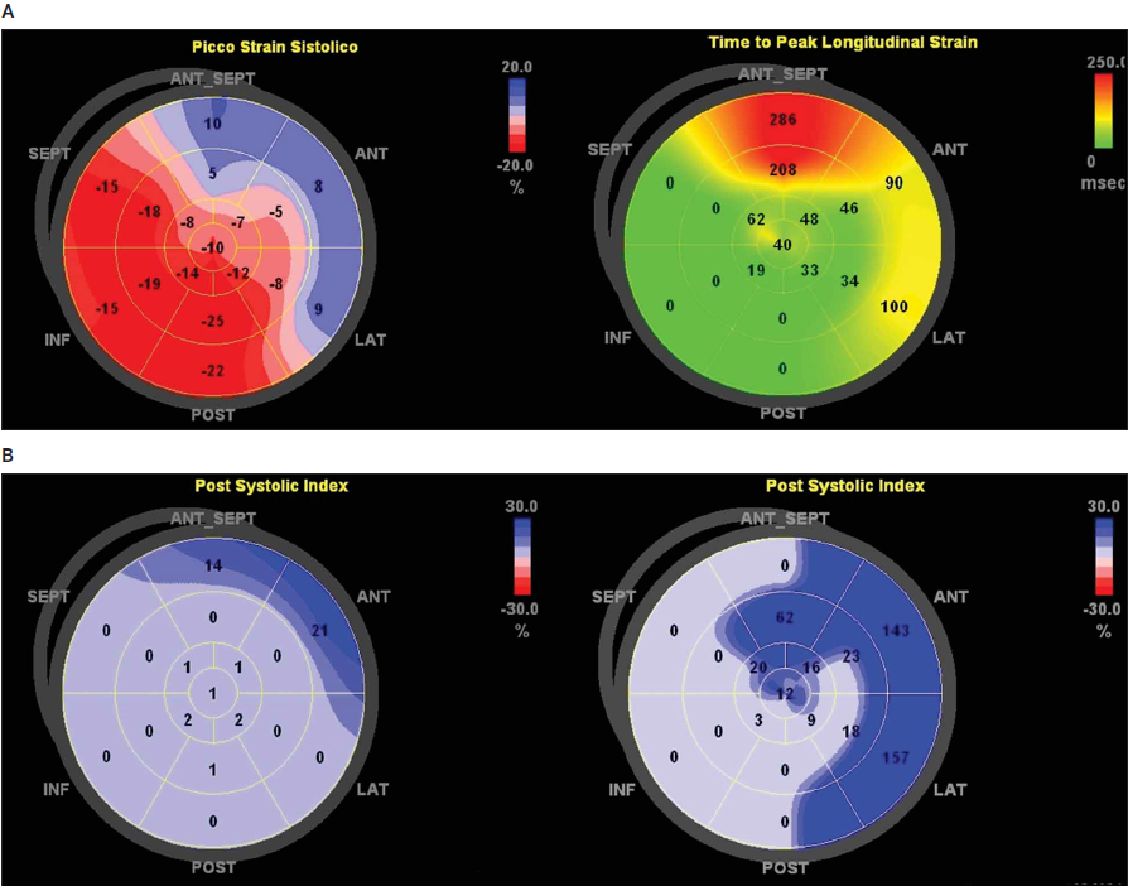
Рис. 3. Топографическое представление (мишень ― bull’s-eye) различных измерений деформации. А ― представлена продольная деформация (слева) и время до пика продольной деформации (справа) у пациента с тяжелым стенозом левой передней нисходящей артерии
Обратите внимание на хроматическую индивидуализацию зоны ишемии (слева), также показана задержка сокращения (красная зона с сокращением задержки 286 мс; справа). B ― измерение постсистолического индекса при speckle-tracking эхокардиографии в начале исследования (слева) и при физической нагрузке (50 Вт; справа) у пациента, подвергающегося эхокардиографии с физической нагрузкой
Обратите внимание на ухудшение задержки сокращения ЛЖ в переднебоковой части. После коронарной ангиографии выявлена патология левой коронарной и левой нисходящей артерий сердца. ANT указывает на передний; ANT_SEPT ― переднеперегородочный; INF ― нижний; LAT ― боковой и POST ― задний.
Лечение при блокаде ножек пучка Гиса
Терапия патологии зависит от вида и электрокардиографических показателей во время диагностики. Особенного лечения при поражении правой ножки пучка чаще всего не требуется. В этом случае больному рекомендуется соблюдать мероприятия, направленные на предотвращение осложнений патологии.
Для этого пациенту следует придерживаться следующих правил:
- закаливаться, обливаться холодной водой;
- адекватно реагировать на стрессы;
- ввести в рацион чаи, включающие успокаивающие травы (валериану, пустырник, бузину, липу, крапиву, душицу);
- отказаться от тяжелой физической работы, занятий силовыми видами спорта;
- соблюдать правильное питание, отказаться от продуктов, повышающих уровень холестерина в крови;
- исключить жирную, острую, жаренную, копченую пищу, майонез, соусы, маринады, кетчупы.
Специфического медикаментозного лечения данного нарушения проводимости нет. Пациенты с блокадой правой ножки пучка Гиса при отсутствии основного заболевания, в лечении не нуждаются. Пациентам с одно- или двухпучковой блокадой для лечения основного заболевания могут быть назначены следующие группы препаратов:
антиоксиданты – убихинон, карнитин, мексидол, предуктал;
витамины – тиамин (витамин В1) с липоевой кислотой, рибофлавин (витамин В2), никотиновая кислота (витамин РР);
седативные препараты растительного происхождения (зверобой, пустырник, валериана, шалфей);
антиагреганты для предупреждения тромбообразования в сердце и в сосудах – аспирин, кардиомагнил, тромбо Асс;
липидснижающие препараты для нормализации уровня холестерина – статины (розувастатин, аторвастатин, симвастатин);
аниангинальные препараты для лечения ишемической болезни сердца – нитраты короткого и продолжительного действия (нитроглицерин, изокет, кардикет, моночинкве);
препараты для лечения заболеваний бронхолегочной системы, вызвавших развитие «легочного» сердца – ингаляционные адреномиметики и глюкокортикостероиды (беротек, беродуал, спирива, беклазон);
гипотензивные средства для лечения артериальной гипертонии – ингибиторы АПФ (периндоприл, лизиноприл), антагонисты рецепторов к ангиотензиногену II (лозартан, валсартан), бета – адреноблокаторы (бисопролол, атенолол), антагонисты кальциевых каналов (амлодипин, верапамил)
Последние две группы должны назначаться с осторожностью, так как уменьшают частоту сердечных сокращений;
антибиотики, нестероидные противовоспалительные препараты при воспалении оболочек сердца – пенициллин; нимесулид, диклофенак;
диуретики и сердечные гликозиды при развитии хронической сердечной недостаточности — индапамид, диувер, лазикс; строфантин, дигоксин.. Кроме медикаментозной, применяется хирургический метод лечения блокады, который заключается в установке пациенту электрокардиостимулятора (ЭКС)
Полная правая блокада, особенно в сочетании с левой гемиблокадой (блокадой одной ветви левой ножки), и полная левая блокада, развившиеся в остром периоде инфаркта миокарда (10 — 14 дней), являются показанием для проведения временной электрокардиостимуляции посредством введения электрода через центральную вену в правый желудочек
Кроме медикаментозной, применяется хирургический метод лечения блокады, который заключается в установке пациенту электрокардиостимулятора (ЭКС). Полная правая блокада, особенно в сочетании с левой гемиблокадой (блокадой одной ветви левой ножки), и полная левая блокада, развившиеся в остром периоде инфаркта миокарда (10 — 14 дней), являются показанием для проведения временной электрокардиостимуляции посредством введения электрода через центральную вену в правый желудочек.
Трехпучковая блокада с полным предсердно – желудочковым блоком, редким ритмом желудочковых сокращений и с приступами Морганьи — Эдемса — Стокса (приступы потери сознания) является показанием для постоянной электрокардиостимуляции (имплантация искусственного водителя ритма или кардиовертера – дефибриллятора).
Формы заболевания СССУ
-
Синусовая брадикардия — ритм с частотой до 60 сокращений в минуту. Считается нормой для физически тренированных лиц, спортсменов, а также молодых людей с превалированием вагусных влияний на сердце. Кроме того, во время сна происходит физиологическое урежение ЧСС на 30%. В иных случаях брадикардия сопровождает различные заболевания.
Умеренная брадикардия может не нарушать кровообращение, однако ритм с частотой менее 40 ударов в минуту приводит к недостаточному кровоснабжению и ишемизации (дефициту кислорода) органов и тканей, нарушая этим их функцию.
Вне зависимости от причины, основа брадикардии — это нарушение способности синусного узла генерировать электрические импульсы с минутной частотой больше 60 либо некорректное их распространение по проводящей системе.
-
Синоатриальная блокада. При данном виде синусной дисфункции происходит торможение вплоть до полной остановки передачи электрической волны от водителя ритма к предсердиям. При этом наблюдается увеличение паузы между сокращениями предсердий, их временная асистолия и как следствие отсутствие своевременного сокращения желудочков, что сказывается на гемодинамике.
Механизм развития блокады бывает связан как блокированием движения импульса от источника, так и с отсутствием формирования возбуждения в самом узле.
- Остановка СУ. Синус-арест грозит внезапной остановки сердечной деятельности. Однако чаще роль источника импульсов берет на себя водитель ритма II порядка (АВ-узел), генерирующий сигналы частотой 40-60 в минуту или III порядка (пучок Гиса, волокна Пуркинье) при АВ-блокаде, частота =15-40 в мин.
ВЫВОДЫ
Speckle-tracking эхокардиография – новая сложная эхокардиографическая техника, которая работает со стандартным 2-мерным изображением, лишенная ограничений доплеровских технологий, обеспечивает всесторонний анализ глобальной и регионарной деформации миокарда во всех пространственных плоскостях. Кроме того, speckle-tracking эхокардиография позволяет оценить ЛЖ ротационную и торсионную динамику – параметры функции ЛЖ, которые до внедрения этой методики, анализировались исключительно с помощью МРТ.
В течение последних 3-х лет растет доказательная база, которая показывает хорошее технико-экономическое обоснование, воспроизводимость и точность speckle-tracking эхокардиографии при различном клиническом применении. Тем не менее, все еще не опубликовано проспективного клинического испытания для оценки этого метода в больших популяциях. Недавно разработанная трехмерная speckle-tracking техника, показала многообещающие предварительные результаты в оценке данных 3-мерных изображений. Это еще одно технологическое направление, которое, предположительно, обеспечит более объемный и подробный анализ сердечной динамики, в результате чего эхокардиография приблизится к самому продвинутому методу визуализации, при этом сохранив возможность ее выполнения у постели больного.
rh.org.ru
- Просмотры:
- Комментарии: